Оксид железа (ii)
Содержание:
- ПРОИСХОЖДЕНИЕ
- Доменный процесс производства чугуна
- ЗАПАСЫ И ДОБЫЧА
- Получение и применение железа
- ТАБЛИЦА Сколько нужно железа в день в миллиграммах (мг)
- Область применения
- Применение
- Получение металла
- Химические свойства железа
- Черные саморезы
- Сфера применения вторичных черных металлов
- Применение железа:
- Список литературы
- Сплавы
- История – краткая справка
- Общие сведения:
- Удаление бактериального железа
- СВОЙСТВА
- Свойства
- Свойства атома железа:
ПРОИСХОЖДЕНИЕ
Самородное железо
Происхождение теллурическое (земное) железо редко встречается в базальтовыхлавах (Уифак, о. Диско, у западного берега Гренландии, вблизи г. Касселя Германия). В обоих пунктах с ним ассоциируют пирротин (Fe1-xS) и когенит (Fe3C), что объясняют как восстановление углеродом (в том числе и из вмещающих пород), так и распадом карбонильных комплексов типа Fe(CO)n. В микроскопических зернах оно не раз устанавливалось в измененных (серпентинизированных) ультраосновных породах также в парагенезисе с пирротином, иногда с магнетитом, за счет которых оно и возникает при восстановительных реакциях. Очень редко встречается в зоне окисления рудных месторождений, при образовании болотных руд. Зарегистрированы находки в осадочных породах, связываемые с восстановлением соединений железа водородом и углеводородами.
Почти чистое железо найдено в лунном грунте, что связывают как с падениями метеоритов, так и с магматическими процессами. Наконец, два класса метеоритов — железокаменные и железные содержат природные сплавы железа в качестве породообразующего компонента.
Доменный процесс производства чугуна
Доменный процесс производства чугуна составляют следующие стадии:
а) подготовка (обжиг) сульфидных и карбонатных руд — перевод в оксидную руду:
FeS2→Fe2O3 (O2,800°С, -SO2) FeCO3→Fe2O3 (O2,500-600°С, -CO2)
б) сжигание кокса при горячем дутье:
С(кокс) + O2 (воздух) →СO2 (600—700°С) СO2 + С(кокс) ⇌ 2СО (700—1000 °С)
в) восстановление оксидной руды угарным газом СО последовательно:
Fe2O3→(CO) (FeIIFe2III)O4→(CO) FeO→(CO) Fe
г) науглероживание железа (до 6,67 % С) и расплавление чугуна:
Fе(т)→(C(кокс) 900—1200°С)Fе(ж) (чугун, t пл 1145°С)
В чугуне всегда в виде зерен присутствуют цементит Fe2С и графит.
ЗАПАСЫ И ДОБЫЧА
Железо — один из самых распространённых элементов в Солнечной системе, особенно на планетах земной группы, в частности, на Земле. Значительная часть железа планет земной группы находится в ядрах планет, где его содержание, по оценкам, около 90 %. Содержание железа в земной коре составляет 5 %, а в мантии около 12 %.

Железо
В земной коре железо распространено достаточно широко — на его долю приходится около 4,1 % массы земной коры (4-е место среди всех элементов, 2-е среди металлов). В мантии и земной коре железо сосредоточено главным образом в силикатах, при этом его содержание значительно в основных и ультраосновных породах, и мало — в кислых и средних породах.
Известно большое число руд и минералов, содержащих железо. Наибольшее практическое значение имеют красный железняк (гематит, Fe2O3; содержит до 70 % Fe), магнитный железняк (магнетит, FeFe2O4, Fe3O4; содержит 72,4 % Fe), бурый железняк или лимонит (гётит и гидрогётит, соответственно FeOOH и FeOOH·nH2O). Гётит и гидрогётит чаще всего встречаются в корах выветривания, образуя так называемые «железные шляпы», мощность которых достигает несколько сотен метров. Также они могут иметь осадочное происхождение, выпадая из коллоидных растворов в озёрах или прибрежных зонах морей. При этом образуются оолитовые, или бобовые, железные руды. В них часто встречается вивианит Fe3(PO4)2·8H2O, образующий чёрные удлинённые кристаллы и радиально-лучистые агрегаты.
Содержание железа в морской воде — 1·10−5-1·10−8 %
В промышленности железо получают из железной руды, в основном из гематита (Fe2O3) и магнетита (FeO·Fe2O3).
Существуют различные способы извлечения железа из руд. Наиболее распространённым является доменный процесс.
Первый этап производства — восстановление железа углеродом в доменной печи при температуре 2000 °C. В доменной печи углерод в виде кокса, железная руда в виде агломерата или окатышей и флюс (например, известняк) подаются сверху, а снизу их встречает поток нагнетаемого горячего воздуха.
Кроме доменного процесса, распространён процесс прямого получения железа. В этом случае предварительно измельчённую руду смешивают с особой глиной, формируя окатыши. Окатыши обжигают, и обрабатывают в шахтной печи горячими продуктами конверсии метана, которые содержат водород. Водород легко восстанавливает железо, при этом не происходит загрязнения железа такими примесями, как сера и фосфор, которые являются обычными примесями в каменном угле. Железо получается в твёрдом виде, и в дальнейшем переплавляется в электрических печах. Химически чистое железо получается электролизом растворов его солей.
Получение и применение железа
Промышленное железо получают выплавкой чугуна и стали.
Чугун — это сплав железа с примесями кремния, марганца, серы, фосфора, углерода. Содержание углерода в чугуне превышает 2% (в стали менее 2%).
Чистое железо получают:
- в кислородных конверторах из чугуна;
- восстановлением оксидов железа водородом и двухвалентным оксидом углерода;
- электролизом соответствующих солей.
Чугун получают из железных руд восстановлением оксидов железа. Выплавку чугуна осуществляют в доменных печах. В качестве источника тепла в доменной печи используется кокс.
Доменная печь является очень сложным техническим сооружением высотой в несколько десятков метров. Она выкладывается из огнеупорного кирпича и защищается внешним стальным кожухом. По состоянию на 2013 год самая крупная доменная печь была построена в Южной Корее сталелитейной компанией POSCO на металлургическом заводе в городе Кванъян (объем печи после модернизации составил 6000 кубометров при ежегодной производительности 5 700 000 тонн).
 Рис. Доменная печь.
Рис. Доменная печь.
Процесс выплавки чугуна в доменной печи идет непрерывно в течение нескольких десятилетий, пока печь не выработает свой ресурс.
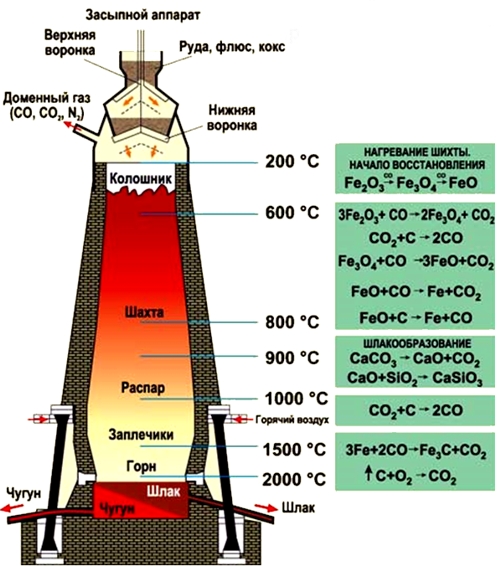 Рис. Процесс выплавки чугуна в доменной печи.
Рис. Процесс выплавки чугуна в доменной печи.
- обогащенные руды (магнитный, красный, бурый железняк) и кокс засыпаются через колошник, расположенный в самом верху доменной печи;
- процессы восстановления железа из руды под действием оксида углерода (II) протекают в средней части доменной печи (шахте) при температуре 450-1100°C (оксиды железа восстанавливаются до металла):
- 450-500°C — 3Fe2O3 + CO = 2Fe3O4 + CO2;
- 600°C — Fe3O4 + CO = 3FeO + CO2;
- 800°C — FeO + CO = Fe + CO2;
- часть двухвалентного оксида железа восстанавливается коксом: FeO + C = Fe + CO.
- параллельно идет процесс восстановления оксидов кремния и марганца (входят в железную руду в виде примесей), кремний и марганец входят в состав выплавляющегося чугуна:
- SiO2 + 2C = Si + 2CO;
- Mn2O3 + 3C = 2Mn + 3CO.
- при термическом разложении известняка (вносится в доменную печь) образуется оксид кальция, который реагирует с оксидами кремния и алюминия, содержащихся в руде:
- CaCO3 = CaO + CO2;
- CaO + SiO2 = CaSiO3;
- CaO + Al2O3 = Ca(AlO2)2.
- при 1100°C процесс восстановления железа прекращается;
- ниже шахты располагается распар, самая широкая часть доменной печи, ниже которой следует заплечник, в котором выгорает кокс и образуются жидкие продукты плавки — чугун и шлаки, накапливающиеся в самом низу печи — горне;
- в верхней части горна при температуре 1500°C в струе вдуваемого воздуха происходит интенсивное сгорание кокса: C + O2 = CO2;
- проходя через раскаленный кокс, оксид углерода (IV) превращается в оксид углерода (II), являющийся восстановителем железа (см. выше): CO2 + C = 2CO;
- шлаки, образованные силикатами и алюмосиликатами кальция, располагаются выше чугуна, защищая его от действия кислорода;
- через специальные отверстия, расположенные на разных уровнях горна, чугун и шлаки выпускаются наружу;
- бОльшая часть чугуна идет на дальнейшую переработку — выплавку стали.
Сталь выплавляют из чугуна и металлолома конверторным способом (мартеновский уже устарел, хотя еще и применяется) или электроплавкой (в электропечах, индукционных печах). Суть процесса (передела чугуна) заключается в понижении концентрации углерода и других примесей путем окисления кислородом.
Как уже было сказано выше, концентрация углерода в стали не превышает 2%. Благодаря этому, сталь в отличие от чугуна достаточно легко поддается ковке и прокатке, что позволяет изготавливать из нее разнообразные изделия, обладающие высокой твердостью и прочностью.
Твердость стали зависит от содержания углерода (чем больше углерода, тем тверже сталь) в конкретной марке стали и условий термообработки. При отпуске (медленном охлаждении) сталь становится мягкой; при закалке (быстром охлаждении) сталь получается очень твердой.
Для придания стали нужных специфических свойств в нее добавляют лигирующие добавки: хром, никель, кремний, молибден, ванадий, марганец и проч.
Чугун и сталь являются важнейшими конструкционными материалами в подавляющем большинстве отраслей народного хозяйства.
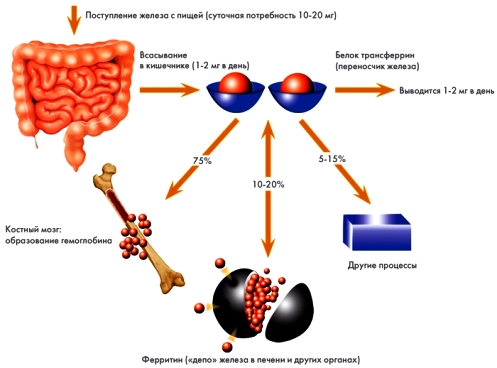
- в организме взрослого человека содержится около 5 г железа;
- железо играет важную роль в работе кроветворных органов;
- железо входит в состав многих сложных белковых комплексов (гемоглобина, миоглобина, различных ферментов).
ТАБЛИЦА Сколько нужно железа в день в миллиграммах (мг)
Область применения
 Сфера использования железа и железных сплавов огромна. Проще указать, где металл не применяется.
Сфера использования железа и железных сплавов огромна. Проще указать, где металл не применяется.
- Строительство – сооружение всех видов каркасов, от несущего каркаса моста, до коробки декоративного камина в квартире, не может обойтись без стали разных сортов. Арматура, прутки, двутавры, швеллеры, уголки, трубы: абсолютно вся фасонная и сортовая продукция используется в строительстве. То же самое касается и листового проката: из него изготавливают кровлю, металлочерепицу, профнастил и так далее.
- Машиностроение – по прочности и стойкости к износу со сталью очень мало, что может сравниться, так что детали корпуса абсолютного большинства машин изготавливаются из сталей. Тем более в тех случаях, когда оборудование должно работать в условиях высоких температур и давления.
- Инструменты – с помощью легирующих элементов и закалки металлу можно придать твердость и прочность близкую к алмазам. Быстрорежущие стали – основа любых обрабатывающих инструментов.
- В электротехнике использование железа более ограничено, именно потому, что примеси заметно ухудшают его электрические свойства, а они и так невелики. Зато металл незаменим в производстве магнитных частей электрооборудования.
- Трубопровод – из стали и чугуна изготавливают коммуникации любого рода и вида: отопление, водопроводы, газопроводы, включая магистральные, оболочки для силовых кабелей, нефтепроводы и так далее. Только сталь способна выдерживать столь огромные нагрузки и внутреннее давление.
- Бытовое использование – сталь применяется везде: от фурнитуры и столовых приборов до железных дверей и замков. Прочность металла и износостойкость делают его незаменимым.
Железо и его сплавы сочетают в себе прочность, долговечностью стойкость к износу. Кроме того, металл относительно дешев в производстве, что и делает его незаменимым материалом для современного народного хозяйства.
Про сплавы железа с цветными металлами и тяжелыми черными расскажет это видео:
Применение
Более 90% всего металлургического производства занимает железо и его сплавы.
Продукция из сталей и чугунов — незаменимая и бóльшая часть конструкционных материалов, а это здания, мосты, железные дороги и многое другое.
Применение соединений железа:
- двух- и трехвалентное железо используют в качестве коагулянта в системах водоочистки;
- аноды в железо-никелевых и железо-воздушных аккумуляторах изготовлены из самого известного черного металла;
- магнетит в виде ультрадисперсного порошка применяют в черно-белых лазерных принтерах;
- FeCl3 применяют радиолюбители (травят печатные платы);
- магнетит незаменим в изготовлении носителей памяти (жесткие диски).

Сферы применения железа
Для большинства организмов без железа нет жизни; при его помощи кислород доставляется к каждой клетке организма. Недостаток железа влечет за собой хлорозы у растений и железодефицитные анемии у животных.
Познавательно: убеждение, что яблоко на разрезе темнеет от входящего в них железа — миф.
Получение металла
Есть несколько способов получения железа:
- Прямые способы. Это производство губчатого железа в шахтных и тоннельных печах. Производство железной крицы во вращающихся печах. Возможно получение железа в реакторах кипящего слоя и химико-термический способ.
- Доменный процесс — распространенный метод. Железная руда и флюс восстанавливаются углеродом кокса, в результате получаем чугун. При надобности из чугуна удаляют примеси (фосфор, сера) и избытки углерода в мартеновских печах или в конвертерах. Легированную сталь получают в электрических печах (ЭПС).
- Химически чистое железо можно получить из раствора его солей с помощью электролиза.
Химические свойства железа
- реагирует с кислородом, в зависимости от температуры и концентрации кислорода могут образовываться различные продукты или смесь продуктов окисления железа (FeO, Fe2O3, Fe3O4): 3Fe + 2O2 = Fe3O4;
- окисление железа при низких температурах: 4Fe + 3O2 = 2Fe2O3;
- реагирует с водяным паром: 3Fe + 4H2O = Fe3O4 + 4H2;
- мелко раздробленное железо реагирует при нагревании с серой и хлором (сульфид и хлорид железа): Fe + S = FeS; 2Fe + 3Cl2 = 2FeCl3;
- при высоких температурах реагирует с кремнием, углеродом, фосфором: 3Fe + C = Fe3C;
- с другими металлами и с неметаллами железо может образовывать сплавы;
- железо вытесняет менее активные металлы из их солей: Fe + CuCl2 = FeCl2 + Cu;
- с разбавленными кислотами железо выступает в роли восстановителя, образуя соли: Fe + 2HCl = FeCl2 + H2;
- с разбавленной азотной кислотой железо образует различные продукты восстановления кислоты, в зависимости от ее концентрации (N2, N2O, NO2).
Черные саморезы
 Черные саморезы
Черные саморезы
Производятся из углеродистой стали. Имеют выраженные отличия от других изделий вследствие приобретения темного оттенка. Методы, позволяющие обеспечить такой эффект, разные.
Цинкование с почернением
Другое название – черное цинкование. Принцип создания поверхностного слоя такой же, что и в случае с изделиями других цветов: получают подобный эффект вследствие хроматирования. Однако в результате образуется покрытие толщиной 0,25-1 мкм. Этот параметр определяет степень защиты от ржавления. Причем рекомендуется приобретать крепежные элементы, прошедшие этап промасливания. Однако все равно для эксплуатации за пределами помещений и в комнатах с высоким уровнем влажности их не применяют.
Технология оксидирования
Целью в данном случае также является обеспечение защиты от коррозии. При этом используется метод оксидирования, когда на металле появляется оксидная пленка. По свойствам изделия этой группы превосходят аналоги ранее рассмотренного вида, но ненамного. Так, за пределами помещений их все же не рекомендуется применять. Можно использовать такой крепеж внутри объектов при условии, что уровень влажности будет низким. Улучшает свойства саморезов, опять же, метод промасливания или гидрофобизация.
Фосфатирование саморезов
Преимуществом фосфатирования является образование более надежного защитного покрытия – толщиной 2-15 мкм. Получают его путем нанесения на саморез порошка Мажеф. Он содержит фосфаты железа, фосфора, марганца. Риск повреждения этого слоя невысокий, что обусловлено внутренними процессами – сцепка порошка с металлом происходит на молекулярном уровне. Как результат, повышается механическая прочность крепежных элементов, а также антикоррозионная стойкость. Фосфатированные саморезы также могут подвергаться гидрофобизации для улучшения свойств. Нужно учитывать, что иногда черный цвет получают изделия в результате окрашивания. Они не могут противостоять воздействию влаги.
Таким образом, при выборе крепежных элементов необходимо учитывать, из какого металла они изготовлены, чем покрыты. По цвету можно предположить, какая технология использовалась для защиты саморезов. Если они будут правильно выбраны, увеличится срок службы всей конструкции, т. к. наиболее надежные крепежные элементы не подвергаются влиянию негативных внешних факторов.
Сфера применения вторичных черных металлов
Благодаря современной технологии переработки из вторичного черного металла производят качественные изделия, которые ничем не уступают аналогам, изготовленным из руды.
Переплавленное сырье ничуть не хуже первичного (полученного из руды), поэтому используется переплавленный металл повсеместно.

Практически любые изделия можно изготовить из вторсырья, что очень выгодно для всей металлургической отрасли.
Народные умельцы часто применяют лом чермета для изготовления полезных в быту предметов. О том, как подарить вторую жизнь отходам металла в домашних условиях, читайте в нашей статье Что можно сделать из отходов черного металла — железа, стали, нержавейки, чугуна.
Применение железа:
- 1. Водород
- 2. Гелий
- 3. Литий
- 4. Бериллий
- 5. Бор
- 6. Углерод
- 7. Азот
- 8. Кислород
- 9. Фтор
- 10. Неон
- 11. Натрий
- 12. Магний
- 13. Алюминий
- 14. Кремний
- 15. Фосфор
- 16. Сера
- 17. Хлор
- 18. Аргон
- 19. Калий
- 20. Кальций
- 21. Скандий
- 22. Титан
- 23. Ванадий
- 24. Хром
- 25. Марганец
- 26. Железо
- 27. Кобальт
- 28. Никель
- 29. Медь
- 30. Цинк
- 31. Галлий
- 32. Германий
- 33. Мышьяк
- 34. Селен
- 35. Бром
- 36. Криптон
- 37. Рубидий
- 38. Стронций
- 39. Иттрий
- 40. Цирконий
- 41. Ниобий
- 42. Молибден
- 43. Технеций
- 44. Рутений
- 45. Родий
- 46. Палладий
- 47. Серебро
- 48. Кадмий
- 49. Индий
- 50. Олово
- 51. Сурьма
- 52. Теллур
- 53. Йод
- 54. Ксенон
- 55. Цезий
- 56. Барий
- 57. Лантан
- 58. Церий
- 59. Празеодим
- 60. Неодим
- 61. Прометий
- 62. Самарий
- 63. Европий
- 64. Гадолиний
- 65. Тербий
- 66. Диспрозий
- 67. Гольмий
- 68. Эрбий
- 69. Тулий
- 70. Иттербий
- 71. Лютеций
- 72. Гафний
- 73. Тантал
- 74. Вольфрам
- 75. Рений
- 76. Осмий
- 77. Иридий
- 78. Платина
- 79. Золото
- 80. Ртуть
- 81. Таллий
- 82. Свинец
- 83. Висмут
- 84. Полоний
- 85. Астат
- 86. Радон
- 87. Франций
- 88. Радий
- 89. Актиний
- 90. Торий
- 91. Протактиний
- 92. Уран
- 93. Нептуний
- 94. Плутоний
- 95. Америций
- 96. Кюрий
- 97. Берклий
- 98. Калифорний
- 99. Эйнштейний
- 100. Фермий
- 101. Менделеевий
- 102. Нобелий
- 103. Лоуренсий
- 104. Резерфордий
- 105. Дубний
- 106. Сиборгий
- 107. Борий
- 108. Хассий
- 109. Мейтнерий
- 110. Дармштадтий
- 111. Рентгений
- 112. Коперниций
- 113. Нихоний
- 114. Флеровий
- 115. Московий
- 116. Ливерморий
- 117. Теннессин
- 118. Оганесон
- https://en.wikipedia.org/wiki/Iron
- https://de.wikipedia.org/wiki/Eisen
- https://ru.wikipedia.org/wiki/Железо
- http://chemister.ru/Database/properties.php?dbid=1&id=236
- https://chemicalstudy.ru/zhelezo-svoystva-atoma-himicheskie-i-fizicheskie-svoystva/
Примечание: Фото https://www.pexels.com, https://pixabay.com
Найти что-нибудь еще?
карта сайта
железо атомная масса степень окисления валентность плотность температура кипения плавления физические химические свойства структура теплопроводность электропроводность кристаллическая решеткаатом нарисовать строение число протонов в ядре строение электронных оболочек электронная формула конфигурация схема строения электронной оболочки заряд ядра состав масса орбита уровни модель радиус энергия электрона переход скорость спектр длина волны молекулярная масса объем атома электронные формулы сколько атомов в молекуле железа сколько электронов в атоме свойства металлические неметаллические термодинамические
Коэффициент востребованности
1 793
Список литературы
- Зарицкий П.В., Довгополов С.Д., Самойлович Л.Г. Состав и генезис рудопроявления самородного железа г. Озёрной в бассейне р. Курейки. — Вестник Харьковского ун-та, 1986, №283 (Средняя Сибирь)
- Мельцер М.А. и др. Самородное железо в золотонсных жилах Аллах-Юньского района и некоторые вопросы их генезиса. — Новые данные по геологии Якутии. Я., 1975, с. 74-78
- Попов В.И. О находках самородного железа в Ср. Азии. — Зап. Узб. отд. ВМО, 1952, в. I
- Сафонов Ю.Г., Генкин А.Д., Романов В.П. и др. Самородное золото, минералы платиновой группы и самородное железо в моренных отложе- ниях Центральной России (Ивановская область). — Геология рудных месторождений, 1997, т. 39, N 3, 289-299.
- Фекличев В.Г., Герасименко В.Я., Спицын А.Н. Техногенное металлическое железо и фосфосилициды железа золоотвалов. — Зап. РМО, 1999, ч.128, вып. 1, с. 50-54
- Palache, Charles, Harry Berman & Clifford Frondel (1944), The System of Mineralogy of James Dwight Dana and Edward Salisbury Dana Yale University 1837-1892, Seventh edition, Volume I: 114-116.
Сплавы
Ориентироваться в море сплавов железа (сталей, чугунов) помогает маркировка. Она поможет определить состав сплава, количество углерода и легирующие элементы, отличить их свойства.
Общую характеристику можно дать по химическому составу: это углеродистая и легированная стали.
Стали делят по применению:
| Вид и марки стали | Применение |
| Строительная Ст0-3 | Вторичные элементы конструкций, малоответственные делали (перила, настилы) |
| Строительная Ст3 | Можно использовать для несущих конструкций, но при плюсовых температурах |
| Конструкционная Ст20 | Малонагруженные детали |
| Легированная 10ХСНД | Используют в сварных конструкциях судо- и вагоностроения, химическом машиностроении |
| Легированная 18ХГТ | Выдерживает ударные нагрузки, высокое давление |
| Легированная 09Г2С | Для работы под давлением, при температурах от -70 до +450 градусов. |
История – краткая справка
Теорий происхождения слова «железо» несколько, которые во многом зависят от региона и наречия.
Русское наименование, к которому мы все привыкли имеет праславянские корни «želězo», которое в свою очередь видимо произошло из греческого «χαλκός», что в переводе означает «железо и медь».
Но как бы там не было, неоспоримый факт один – применение железа осуществлялось еще в 4 тысячелетии до н.э., т.к. именно этого периода были найдены древние изделия из этого материала.
Популярными историческими изделиями являются украшения из египетских гробниц (более 3000 до н.э.) и кинжал из древнего города Ур (Шумер), откуда согласно Священным Писанием Бог призвал выйти Авраама.
Первый народ, которые начали плавить Fe – хатты, которые проживали на территории Юго-Восточной сегодняшней Турции примерно в 2000 до н.э. Эти сведения археологи получили из древних текстов царя хеттов Анитты, завоевавшего со своим народом хаттов.
Первые сведения о получении из железа стали появились в записях Аристотеля, из легенды об аргонавтах. Народ «Халибы» тщательно промывали речной песок, отсеивая из него тяжелые фракции гематита и магнетита, которые затем в печи переплавляли до получения серебристого нержавеющего металла.
Общие сведения:
| 100 | Общие сведения | |
| 101 | Название | Железо |
| 102 | Прежнее название | |
| 103 | Латинское название | Ferrum |
| 104 | Английское название | Iron |
| 105 | Символ | Fe |
| 106 | Атомный номер (номер в таблице) | 26 |
| 107 | Тип | Металл |
| 108 | Группа | Амфотерный, переходный, чёрный металл |
| 109 | Открыт | Известно с глубокой древности |
| 110 | Год открытия | до 5000 года до н.э. |
| 111 | Внешний вид и пр. | Ковкий, вязкий металл серебристо-белого цвета с сероватым оттенком |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | 5 аллотропных модификации железа:
— α-железо (феррит) с кубической объемно-центрированной кристаллической решёткой и свойствами ферромагнетика, — β-железо с кубической объёмно-центрированной кристаллической решёткой, отличающееся от α-железа параметрами кристаллической решётки и свойствами парамагнетика. β-железо служит для обозначения α-железа выше точки Кюри (точка Кюри железа 769 °C), — γ-железо (аустенит) с кубической гранецентрированной кристаллической решёткой, — δ-железо с кубической объёмно-центрированной кристаллической решёткой, — ε-железо с гексагональной плотноупакованной кристаллической решёткой |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга* | |
| 116 | Конденсат Бозе-Эйнштейна | |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 6,3 % |
| 120 | Содержание в морях и океанах (по массе) | 3,0·10-7 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 0,11 % |
| 122 | Содержание в Солнце (по массе) | 0,1 % |
| 123 | Содержание в метеоритах (по массе) | 0,22 % |
| 124 | Содержание в организме человека (по массе) | 0,006 % |
Удаление бактериального железа
При наличии в исходной воде большого количества железа пользователь может столкнуться еще с одной проблемой — появлением бактериальных загрязнений — активным развитием железобактерий.Если проблема железобактерий выявлена на ранней стадии, регулярное хлорирование или обработка хелатными агентами (органические вещества, образующие растворимые комплексы с железными отложениями), а также постоянное наблюдение за состоянием оборудования помогут минимизировать её последствия.
На ранней стадии появления железобактерий может помочь ударное хлорирование — необходимо создать избыточную концентрацию хлора 50 мг/л. Перед применением хлорирования нужно выяснить, насколько устойчиво к хлору установленное водоочистное оборудование.
Проблему с бактериальным железом может решить среда redox, однако, в подводящих трубопроводах при этом железобактерии будут продолжать развиваться и образовывать слизистые отложения.
СВОЙСТВА
Железная руда
В чистом виде при нормальных условиях это твердое вещество. Оно обладает серебристо-серым цветом и ярко выраженным металлическим блеском. Механические свойства железа включают в себя уровень твердости по шкале Мооса. Она равна четырем (средняя). Железо обладает хорошей электропроводностью и теплопроводностью. Последнюю особенность можно ощутить, дотронувшись до железного предмета в холодном помещении. Так как этот материал быстро проводит тепло, он за короткий промежуток времени забирает большую его часть из вашей кожи, и поэтому вы ощущаете холод.
Дотронувшись, к примеру, до дерева, можно отметить, что его теплопроводность намного ниже. Физические свойства железа — это и его температуры плавления и кипения. Первая составляет 1539 градусов по шкале Цельсия, вторая — 2860 градусов по Цельсию. Можно сделать вывод, что характерные свойства железа — хорошая пластичность и легкоплавкость. Но и это еще далеко не все. Также в физические свойства железа входит и его ферромагнитность. Что это такое? Железо, магнитные свойства которого мы можем наблюдать на практических примерах каждый день, — единственный металл, обладающий такой уникальной отличительной чертой. Это объясняется тем, что данный материал способен намагничиваться под действием магнитного поля. А по прекращении действия последнего железо, магнитные свойства которого только что сформировались, еще надолго само остается магнитом. Такой феномен можно объяснить тем, что в структуре данного металла присутствует множество свободных электронов, которые способны передвигаться.
Свойства
Железо (Ferrum, в формулах обозначается Fe) — химически активный элемент, относится к металлам. В таблице Менделеева имеет атомный № 26. Ferrum — черный металл.
Физические характеристики сильно зависят от чистоты металла.
Важно: нужно отличать вредные примеси от полезных. Так, фосфор и сера ухудшают характеристики железа
Углерод улучшает твердость и механическую прочность.
Железо имеет 4 модификации; их различие в структуре и кристаллической решетке.
| Свойства атома | |
| Название, символ, номер | Железо / Ferrum (Fe), 26 |
| Атомная масса (молярная масса) | 55,845(2) а. е. м. (г/моль) |
| Электронная конфигурация | 3d6 4s2 |
| Радиус атома | 126 пм |
| Химические свойства | |
| Ковалентный радиус | 117 пм |
| Радиус иона | (+3e) 64 (+2e) 74 пм |
| Электроотрицательность | 1,83 (шкала Полинга) |
| Электродный потенциал | Fe←Fe3+ −0,04 В Fe←Fe2+ −0,44 В |
| Степени окисления | 6, 3, 2, 0 |
| Энергия ионизации (первый электрон) | 759,1 (7,87) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 7,874 г/см³ |
| Температура плавления | 1812 K (1538,85 °C) |
| Температура кипения | 3134 K (2861 °C) |
| Уд. теплота плавления | 247,1 кДж/кг 13,8 кДж/моль |
| Уд. теплота испарения | ~6088 кДж/кг ~340 кДж/моль |
| Молярная теплоёмкость | 25,14 Дж/(K·моль) |
| Молярный объём | 7,1 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая объёмноцентрированная |
| Параметры решётки | 2,866 Å |
| Температура Дебая | 460 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 80,4 Вт/(м·К) |
| Номер CAS | 7439-89-6 |
Рекомендуем: РТУТЬ — «кровь дракона» в лампах и реакторах
Химические свойства железа:
- Степени окисления +2, +3.
- В присутствии влаги воздуха корродирует, причем слой ржавчины не мешает дальнейшему разрушению металла. Постоянной формулы ржавчина не имеет, общая ее формула Fe2O3·x H2O.
- Концентрированные растворы H2SO4 и HNO3 пассивируют поверхность железа, образуют оксидную пленку.
- При взаимодействии с неметаллами образуют нитриды, фосфиды, силициды, карбиды железа.
- Реагирует с металлами, восстанавливая их из растворов солей.
- Железная кислота в свободном виде не существует; ее соли — ферраты — обладают сильными окислительными свойствами. Эти свойства используют для обеззараживания воды.
Свойства атома железа:
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 55,845(2) а.е.м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 3d6 4s2 |
| 203 | Электронная оболочка |
K2 L8 M14 N2 O0 P0 Q0 R0 |
| 204 | Радиус атома (вычисленный) | 156 пм |
| 205 | Эмпирический радиус атома* | 140 пм |
| 206 | Ковалентный радиус* | 123 пм – low-spin,
152 пм – high-spin |
| 207 | Радиус иона (кристаллический) | Fe2+ low spin
75 (6) пм, Fe3+ low spin 69 (6) пм, Fe4+ low spin 72,5 (6) пм, Fe6+ low spin 39 (4) пм, Fe2+ high spin 92 (6) пм, Fe3+ high spin 78,5 (6) пм (в скобках указано координационное число – характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле) |
| 208 | Радиус Ван-дер-Ваальса | |
| 209 | Электроны, Протоны, Нейтроны | 26 электронов, 26 протонов, 30 нейтронов |
| 210 | Семейство (блок) | элемент d-семейства |
| 211 | Период в периодической таблице | 4 |
| 212 | Группа в периодической таблице | 8-ая группа (по старой классификации – побочная подгруппа 8-ой группы) |
| 213 | Эмиссионный спектр излучения |  |