Жир
Содержание:
Классификация
Жиры являются сложными соединениями, которые могут встречаться в разных модификациях, они выполняют разные функции
Они представляют особую важность для клеток, принимают участие в многочисленных процессах человеческого организма. По этой причине классификация липидов достаточно обширная, она включает множество видов жиров, их основные признаки
Ниже в таблице имеется полная классификация жиров в зависимости от строения.
Описанные жиры относятся к омыляемым, во время их гидролиза получается мыло. Отдельно в группу неомыляемых жиров, а именно не вступающих в реакцию с водой, включают стероиды.
В зависимости от строения стероиды подразделяют на подгруппы:
- Стерины. Это стероидные спирты. Они содержатся в составе животных и растительных тканей (холестерин, эргостерин).
- Желчные кислоты. Производные холевой кислоты. Они содержат одну группу –СООН. Обеспечивают полноценное растворение холестерина и переваривание липидов. К этой группе можно отнести такие виды жирных кислот, как холевая, дезоксихолевая, литохолевая.
- Стероидные гормоны. Обеспечивают усиленный рост и развитие организма. К этой группе относятся гормоны – кортизол, тестостерон, кальцитриол.
Существует большая группа – липопротеины. Это сложные соединения жиров и белков (аполипопротеинов). Липопротеины относятся к сложным белкам, но не к жирам.
В их составе имеются разнообразные сложные эфиры:
- холестерины;
- фосфолипиды;
- нейтральные жиры;
- жирные кислоты.
Выделяют две группы липопротеинов:
- Растворимые. Содержатся в плазме крови, молоке, желтке.
- Нерастворимые. Имеются в составе плазмалеммы, оболочки нервных волокон, хлоропластов.
Жиры в зависимости от физической структуры разделяют на твердые, жиры, масла. По нахождению в организме выделяют резервные (непостоянные, зависят от питания) и структурные (генетические обусловленные) жиры. В соответствии с происхождением бывают животными и растительными.
Биохимические методы исследования
Биохим, определение Л. проводится гл. обр. в плазме или сыворотке крови, значительно реже в кале (с целью диагностики стеатореи) и моче (при липурии). Определение Л
в плазме крови особенно важно при заболеваниях, сопровождающихся повышением их концентрации в крови (гиперлипидемиях). К ним относятся некоторые заболевания печени (острые и хрон, гепатиты, цирроз и др.), липоидный нефроз (нефротическая гиперлипидемия), сахарный диабет, атеросклероз, панкреатиты, гипотиреоз
Широко применяется определение Л. (холестерина и триглицеридов) в крови при фенотипировании первичных и вторичных гиперлипопротеинемий с целью диагностики и рационального диетического и медикаментозного лечения. Снижение содержания Л. в крови (гиполипидемия) наблюдается реже — при длительном голодании или резко ограниченном потреблении жиров и при гипертиреозе.
При исследовании Л. в крови необходимо строго придерживаться следующих общих принципов: 1) взятие крови производится натощак спустя 10—12 час. после последнего приема пищи; 2) плазма (сыворотка) крови, используемая для анализа, не должна быть гемолизированной; 3) для экстрагирования Л. применяются органические растворители высокой степени очистки; 4) стандарты или референтные препараты Л. сопоставляют с международными стандартами и хранят в замороженном состоянии.
Существует несколько методов определения общих Л. в плазме (сыворотке) крови. Широкое применение нашли гравиметрические методы, основанные на экстрагировании Л. из плазмы крови смесью органических растворителей, с последующим их выпариванием и взвешиванием липидного остатка. Эти методы, однако, не отличаются высокой точностью.
Ряд методов основан на окислении общих Л. хромовой кислотой с последующим титриметрическим или колориметрическим количественным определением (см. Колориметрия, Титриметрический анализ). Широко применяется метод, основанный на цветной реакции, к-рую дают продукты распада Л. с сульфофосфованилиновым реактивом. Метод определения общих Л. в сыворотке крови с сульфофосфованилиновым реактивом принят у нас в стране в качестве унифицированного; содержание Л. в сыворотке крови здорового человека, определенное этим методом, в среднем составляет 350—800 мг%.
Концентрацию общих Л. в сыворотке крови определяют также методом Свана в модификации Л. К. Баумана (окрашенные судаковым черным Л. количественно извлекаются из сыворотки крови и определяются фотометрически) и турбидиметрическим методом (метод Хуэрго), в основу к-рого положено измерение оптической плотности жировой эмульсии, образуемой при взаимодействии серной к-ты с n-диоксановым экстрактом Л. сыворотки крови. Методом Хуэрго в сыворотке крови здорового человека определяется 500 — 700 мг% общих Л.
Для определения триглицеридов наиболее часто применяют методы, в основе которых лежит гидролитическое расщепление триглицеридов. Образовавшийся в результате гидролиза глицерин окисляют до формальдегида и последний определяют колориметрически. Наибольшей точностью из таких методов обладает метод Карлсона, часто применяемый в модификации Игнатовской (H. Ignatowsca).
Для определения холестерина используют методы, основанные на цветной реакции Либерманна— Бурхарда (см. Либерманна-Бурхарда реакция), причем наибольшей точностью из них обладает метод Абелля (см. Абелля метод). Кроме того, для определения холестерина и триглицеридов в крови начинают применять высокоспецифические энзиматические методы с использованием готовых наборов реактивов. Наконец, для определения этих Л. используют автоанализаторы — отечественный прибор АБМ-1, автоанализатор АА-2 фирмы «Техникой» и др. (см. Автоанализаторы).
Методы определения фосфолипидов основаны на экстрагировании или осаждении фосфолипидов из плазмы (сыворотки) крови, минерализации фосфолипидного фосфора, проведении цветной реакции на фосфор и колориметрическом измерении интенсивности окраски (см. Блура метод).
Для определения неэтерифицированных жирных к-т используют титриметрические и колориметрические методы. Из последних наиболее часто применяют методы, основанные на том, что жирные к-ты образуют с медью соли, которые в свою очередь образуют цветные комплексы с диэтил дитиокарбаматом натрия и другими соединениями.
Для разделения Л. используют методы тонкослойной хроматографии, часто с последующим анализом жирных к-т с помощью газожидкостной хроматографии (см. Хроматография).
Липиды в составе диеты человека
Среди липидов в диетическом питании человека обычно используются триглицериды – нейтральные жиры. Они являются богатым источником энергии, а также они требуются для всасывания витаминов с жирорастворимой структурой.
Насыщенные кислоты имеются в составе следующей пищи:
- различных видов мяса – говядины, свинины, баранины, птицы;
- молочных продуктов;
- некоторых тропических фруктов, а именно кокосов.
Ненасыщенные виды кислот могут попадать в организм человека при употреблении следующих видов продуктов:
- орехов;
- семечек подсолнечника;
- оливкового и других растительных масел.
Главными источниками холестерола в рационе является мясо, внутренние органы животных, яичные желтки, молочные продукты, рыба.
Для справки! Организация American Heart Association советует потреблять липиды в количестве не больше 30% от общего рациона. При диете стоит уменьшить содержание насыщенных кислот до 10% от всех жиров. Не нужно принимать больше 300 мг холестерола в сутки (этот объем входит в состав одного яичного желтка).
Липиды – важные элементы, которые имеют огромное значение для природы и человека. Данные вещества обладают сложным составом, а их классификация объединяет множество групп и подгрупп, которые обладают разными свойствами и отличительными функциями.
Липиды функции. Биологические функции липидов
- Энергетическая. В количественном отношении липиды – основной энергетический резерв организма. Они содержатся в клетках в виде жировых капель, служащих «метаболическим топливом». Липиды окисляются в митохондриях до воды и диоксида углерода с образованием большого количества АТФ .
При полном окислении 1 г жиров до углекислого газа и воды выделяется около 39 кДж энергии, что намного больше по сравнению с полным окислением такого же количества углеводов. Это дает возможность животным, впадающим в спячку, расходовать накопленные летом и осенью жировые запасы для поддержания процессов жизнедеятельности в зимний период. Высокое содержание липидов в семенах растений обеспечивает энергией развитие зародыша и проростка, пока он не перейдет к самостоятельному питанию.
- Структурная (строительная). Ряд липидов принимает участие в построении клеточных мембран. Типичными мембранными липидами являются фосфолипиды, гликолипиды и холестерин. Интересно, что мембраны совсем не содержат жиров.
- Изолирующая (защитная). Жировые отложения в подкожной ткани и вокруг различных органов обладают высокими теплоизолирующими свойствами, благодаря тому, что жиры плохо проводят тепло. У синего кита толщина подкожного жирового слоя превышает 50 см, доходя до 1 м, поэтому он может жить в холодных водах.
Липиды предохраняют внутренние органы от механических повреждений (например, почки человека покрыты жировым слоем, защищающим их от травм, сотрясения при ходьбе и прыжках), так они выполняют роль амортизатора.
Как основной компонент клеточной мембраны липиды изолируют внутреннюю часть клетки от окружающей среды и за счёт гидрофобных свойств обеспечивают образование мембранных потенциалов.
Воск покрывает тонким слоем листья растений, не давая им намокать во время обильных дождей, препятствуя испарению воды в жарком климате.
У водоплавающих птиц и некоторых зверей воски выделяются специальными железами и служат смазкой для перьев и волос, придавая им водоотталкивающие свойства.
Миелиновые липиды в мембранах шванновских клеток образуют оболочку вокруг аксонов нейронов, за счёт этого мембрана поверхности нервной клетки электрически изолируется и импульсы по ней проходят намного быстрее.
- Сигнальная (регуляторная). Стероиды, эйкозаноиды и некоторые метаболиты фосфолипидов выполняют сигнальные функции. Они служат в качестве гормонов, медиаторов и вторичных переносчиков (мессенжеров). Половые гормоны и кортикостероиды регулируют процессы развития и размножения, обмена веществ.
Витамины группы D, которые являются производными холестерина, играют важную роль в обмене кальция и фосфора. Другие витамины липидной природы: А, Е, К. Желчные кислоты участвуют в пищеварении: они обеспечивают эмульгирование жиров пищи и всасывание продуктов их расщепления.
- Запасающая. Жиры служат источником энергии и воды в клетках. Они хранятся в жировых депо: капли жира внутри клетки, жировые тела насекомых, подкожная клетчатка. При окислении 100 г жиров выделяется 107 мл воды. Благодаря эндогенному образованию воды в пустыне могут жить многие животные, например песчанки и тушканчики. С этим связано накопление жира в горбах верблюда.
Развитие эмбрионов птиц и рептилий в яйце при запасе энергии и воды в виде жира, образуется в результате окисления из запасов в желтке. Киты не могут пить солёную воду, которой они окружены, и полагаются полностью на метаболическую воду.
- Другие функции липидов. Отдельные липиды выполняют роль «якоря», удерживающего на мембране белки и другие соединения. Некоторые являются кофакторами, принимающими участие в ферментативных реакциях, например в свёртывании крови или в трансмембранном переносе электронов.
Светочувствительный каротиноид ретиналь играет центральную роль в процессе зрительного восприятия.
Жиры способствуют плавучести водных животных от мельчайших диатомовых водорослей, до китов.
Поскольку некоторые липиды не синтезируются в организме человека, они должны поступать с пищей в виде незаменимых жирных кислот и жирорастворимых витаминов. (рис.) Ненасыщенные жирные кислоты – арахидоновая, линолевая и линоленовая. Линолевая и линоленовая кислоты могут превращаться в арахидоновую за счёт наращивания цепи и, следовательно, являются её заменителями.
Гистохимические методы определения в тканях
Самым старым методом окрашивания Л. в тканях является метод с использованием четырехокиси осмия (OsO4). Этот реактив восстанавливается непредельными жирными к-тами и целым рядом других веществ, обладающих восстанавливающими свойствами. Продукты восстановления OsO4 окрашены в черный цвет. Однако следует признать, что методы выявления Л. с помощью жирорастворимых красителей более просты и надежны. В гистохимии для этих целей прежде всего стали использовать судан III, несколько позже — судан IV и шарлах. Л. более интенсивно окрашиваются красящими смесями, особенно теми, которые содержат два (или более) гомолога или изомера нафтоловых суданов. Окрашивание Л. жирорастворимыми красителями основано на том, что они растворяются в жировых веществах лучше, чем в обычных растворителях. Термин «суданофилия» означает способность ткани окрашиваться любыми жирорастворимыми красителями.
Для сохранения Л. в тканях при фиксации рекомендуется использовать 10 — 15% р-р формалина, но еще лучше использовать фиксатор формол-кальций по Бейкеру: формалин— 10 мл; 10% хлористый кальций — 10 мл; дистиллированная вода — 80 мл.
К этому фиксатору должен быть добавлен мел, для того чтобы смесь имела нейтральную реакцию. Фиксировать ткань рекомендуется 24—48 час., более длительная фиксация может привести к образованию кристаллов, изменению растворимости Л. и т. д. Отмытая после фиксации ткань промывается в проточной воде; срезы готовятся на замораживающем микротоме. Ткань паренхиматозных органов можно предварительно заключить в желатину.
При окрашивании ткани на Л. дает хорошие результаты и одновременно выявляет суданофильную зернистость в сегментоядерных лейкоцитах метод Гольдмана. Р-р судана III для окраски тканей по этому методу готовится следующим образом: 70% этанол — 100 мл; дистиллированная вода —- 20 мл; альфа-нафтол — 1,2 г; судан III — в избытке.
Смесь кипятят в течение 10 мин. и фильтруют. Срезы ткани красят 15 мин., затем дифференцируют в 70% этаноле, контролируя процесс под микроскопом. Мазки крови фиксируют 3 мин. смесью, состоящей из 1 части формалина и 4 частей 96 % этанола.
При окраске тканей на Л. по методу Чаччо следует маленькие кусочки фиксировать в течение 24—48 час. в смеси следующего состава: 5% водный р-р двухромовокислого калия — 80 мл; формалин — 20 мл; ледяная уксусная к-та — 5 мл.
Затем кусочки ткани выдерживают 5 — 8 дней в 3% двухромовокислом калии («хромируют»), сутки промывают в проточной воде, проводят через этанол восходящих концентраций в течение суток, проводят через ксилол и заключают в парафин. Приготовленные срезы после обработки 70% этанолом красят насыщенным р-ром судана III в 70% этаноле или при температуре 50° красителем следующего состава: 80 % этанол — 95 мл; ацетон — 5 мл; судан III — до насыщения.
После охлаждения жидкость фильтруется. Срезы красят 30 — 60 мин. при температуре 30°, споласкивают 50% этанолом, промывают в дистиллированной воде и заключают в глицерин-желатину.
Ядра клеток можно красить на Л. квасцовым гематоксилином, лучше это делать до обработки срезов су-даном. Л. окрашиваются в оранжевокрасный цвет.
Библиография: Алимова Е. К., Аствацатурьян А. Т. и Жаров Л. В. Липиды и жирные кислоты в норме и при ряде патологических состояний, М., 1975; Биохимические методы исследования в клинике, под ред. А. А. Покровского, М., 1969; Кейтс М. Техника липидологии, пер. с англ., М., 1975; Комаров Ф. И., Коровкин Б. Ф. и Меньшиков В. В. Биохимические исследования в клинике, Л., 1976; Липиды, под ред. С. Е. Северина, М., 1977; Меркулов Г. А. Курс патологогистологической техники, с. 241, Л., 1969; П и р с Э. Гистохимия, пер., с англ., с, 259, М., 19 62; Lipids, ed. by R. Paoletti а. о., v. 1—2, N. Y., 1976; Masoro E. J. Physiological chemistry of lipids in mammals, Philadelphia, 1968; Searcy R. L. Lipopa-thies, Springfield, 1971.
Нейтральные липиды
Нейтральные липиды представляют собой сложные эфиры высших жирных кислот и спиртов (высших одноатомных, глицерина, холестерина и др). Наиболее важными из них являются триацилглицериды и воски.
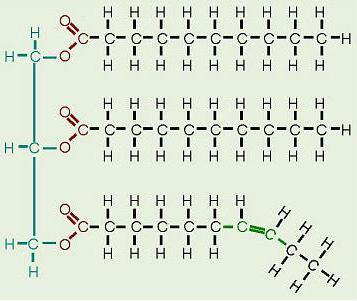
Триацилглицериды
Триацилглицериды – это сложные эфиры глицерина и высших жирных кислот.
Общая формула:
Простые триацилглицериды содержат остатки одинаковых, смешанные – разных жирных кислот. Названия триацилглицеридов строятся на основе названий ацильных остатков, входящих в их состав жирных кислот.
Смешанные триацилглицериды могут содержать хиральный атом углерода в положении 2 и иметь энантиомеры, например:
Для их обозначения используется стереоспецифическая нумерация (sn). Если в проекции Фишера группа ОН (или ее производное) при С2находятся слева, то атому С над ней присваивается номер 1, а под ней – номер 3 и наоборот, например:
Триацилглицериды – малополярные, не растворимые в воде вещества, так как их молекулы не содержат сильнополярных или заряженных групп. Триацилглицериды, содержащие преимущественно остатки ненасыщенных кислот, при обычных условиях являются жидкостями, насыщенных кислот – твердыми веществами. Они входят в состав животных жиров и растительных масел, которые представляют собой смеси триацилглицеридов. Животные жиры содержат в основном триацилглицериды с остатками насыщенных кислот и поэтому имеют твердую консистенцию. Растительные масла включают в основном остатки ненасыщенных кислот и являются жидкостями. Основная биологическая функция триацилглицеридов – запасные вещества животных и растений.
Химические свойства триацилглицеридов определяются наличием сложноэфирной связи и ненасыщенностью. Как сложные эфиры триацилглицериды гидролизуются под действием кислот и щелочей, а также вступают в реакцию переэтерификации.
При щелочном гидролизе (омылении) жиров образуются соли жирных кислот (мыла). Их молекулы дифильны (содержат полярную “голову” и неполярный “хвост”), что обуславливает их повехностно-активные свойства и моющее действие.
По реакции переэтерификации получают смеси сложных эфиров жирных кислот, которые в отличие от самих кислот легко летучи и могут быть разделены путем перегонки или газожидкостной хроматографии. Далее путем гидролиза их превращают в индивидуальные карбоновые кислоты или используют в виде эфиров, например, в качестве лекарственных препаратов, восполняющих недостаток незаменимых жирных кислот в организме (лекарственный препарат линетол ).
Триацилглицериды, содержащие остатки ненасыщенных жирных кислот, вступают в реакции присоединения по двойной связи.
Реакция присоединения галогенов используется для определения содержания остатков ненасыщенных кислот в жирах. Количественной характеристикой степени ненасыщенности жиров служит иодное число – количество иода (в г), которое могут поглотить 100 г жира. У животных жиров иодное число меньше 70, у растительных масел больше 70.
Важным промышленным процессом является гидрогенизация жиров – каталитическое гидрирование растительных масел, в результате которого водород насыщает двойные связи, и жидкие масла превращаются в твердые жиры (маргарин). В процессе гидрогенизации происходит также изомеризация – перемещение двойных связей (при этом из полиненасыщенных кислот образуются кислоты с реакционноспособными, в том числе и в реакциях окисления, сопряженными двойными связями) и изменение их стереохимической конфигурации ( цис в транс ), а также частичное расщепление сложноэфирных связей. Существует мнение, что при этом образуются вещества небезопасные для организма. Наибольшей пищевой ценностью обладают растительные масла, которые наряду с незаменимыми жирными кислотами содержат необходимые для организма фосфолипиды, витамины, полезные фитостерины (предшественники витамина D) и практически не содержат холестерин.
Воски
Воски – это сложные эфиры жирных кислот и высших одноатомных спиртов (С12– С46). Воски входят в состав защитного покрытия листьев растений и кожи человека и животных
Они придают поверхности характерный блеск и водоотталкивающие свойства, что важно для сохранения воды внутри организма и создания барьера между организмом и окружающей средой