Спинальная мышечная атрофия у детей
Содержание:
- Классификация
- Промежуточные данные 3-й фазы STR1VEпо состоянию на 27 сентября 2018 г. (дата среза данных для анализа)
- Причины
- Биохимические исследования
- Диагностика
- Как диагностируют данную патологию?
- Екатерина Мартынова, мама Артёма
- Диагностика и лечение болезни Верднига-Хофмана
- Симптомы заболевания
- Диета при спинальной амиотрофии
- Симптомы у ребёнка и взрослого
- Лечение
- Помогающие организации
Классификация
Спинальные амиотрофии имеют широкий спектр тяжести, проявляясь как у младенцев, так и у взрослых людей. Наиболее часто используемая классификация выглядит следующим образом:
| Тип | Название | Возраст обнаружения | Характеристика |
| SMA1 | Болезнь Верднига-Гоффмана | 0-6 месяцев | Тяжелая форма проявляется в первые месяцы жизни, как правило, с быстрым и неожиданным началом («синдром гибкого ребенка»). Быстрая гибель моторных нейронов вызывает снижение функции основных органов тела, особенно дыхательной системы, а дыхательная недостаточность, вызванная пневмонией, является наиболее частой причиной смерти. Если детей с диагнозом спинальная амиотрофия типа 1 не помещают на искусственную вентиляцию легких, они, как правило, не доживают до двухлетнего возраста, при этом смерть наступает в течение нескольких недель в наиболее тяжелых случаях (иногда это называют СМА типа 0). Известно, что при надлежащей респираторной поддержке больные с более легкой СМА типа I, на долю которых приходится около 10% случаев, доживают до подросткового или даже взрослого возраста. |
| SMA2 | Болезнь Дубовица | 6-18 месяцев | Промежуточная форма поражает детей. К сожалению, ходить или стоять они не смогут, но сохранять положение сидя хотя бы некоторую часть жизни возможно. Наступление слабости обычно отмечается через 6–18 месяцев после рождения. Прогрессирование сильно различается, некоторые дети постепенно становятся слабее, в то время как другие благодаря тщательному уходу дольше не сталкиваются с проблемами. У этих детей может быть сколиоз, и его коррекция при помощи ортопедических устройств поможет дыханию. Мышцы тела ослаблены, что ведет к серьезным проблемам с дыханием. Ожидаемая продолжительность жизни снижается, но большинство людей, у которых спинальная амиотрофия 2 типа, доживают до зрелого возраста. |
| SMA3 | Кугельберга-Веландера | 12 месяцев и более | Ювенильная спинальная амиотрофия обычно проявляется у детей старше года. Они могут ходить без поддержки в течение некоторого времени, хотя многие позже теряют эту способность. Вовлеченность дыхательный системы в заболевание минимальна, а ожидаемая продолжительность жизни нормальная или почти нормальная. |
| SMA4 | — | Только у взрослых | Взросла форма (иногда классифицируемая как СМА3 с поздним началом) обычно проявляется после третьего десятилетия жизни с постепенным ослаблением мышц – в основном поражает проксимальные мышцы конечностей. В связи с этим нередко больные вынуждены перемещаться на инвалидной коляске. Другие осложнения редки, и продолжительность жизни не изменяется. |
Наиболее тяжелую форму спинальной атрофии типа I иногда называют СМА типа 0 (или тяжелая детская форма) и диагностируется у детей, которые родились настолько слабыми, что могут прожить всего несколько недель даже при интенсивной респираторной поддержке. СМА типа 0 не следует путать с СМАРД (спинальная мышечная атрофия с респираторным дистрессом), у которой могут быть очень похожие симптомы и течение, но генетическая причина отличается от спинально-мышечной атрофии.
Моторное развитие у людей, которые имеют спинальные амиотрофии, обычно оценивается с использованием проверенных функциональных шкал – CHOP INTEND (разработанная в Филадельфии), либо шкала измерения двигательной функции, либо один из нескольких вариантов шкалы Хаммерсмит.

Промежуточные данные 3-й фазы STR1VEпо состоянию на 27 сентября 2018 г. (дата среза данных для анализа)
STR1VE — это продолжающееся открытое простое многоцентровое исследование с однократной дозой, предназначенное для оценки эффективности и безопасности однократного внутривенного введения Zolgensmaу пациентов с СМА 1-го типа, которые на момент генной терапии не достигли возраста шести месяцев. Исследование было разработано для охвата как можно более широкой популяции пациентов с СМА 1-го типа с одной или двумя копиями резервного гена SMN2, которые имеют биаллельную делецию гена SMN1 или точечные мутации. Эти критерии хорошо соответствуют популяции пациентов, которые были зарегистрированы в основном испытании 1-й фазы START, при этом потенциально предоставляя лечение некоторым из более редких субпопуляций на исследовательской основе. Исследование STR1VEпланируется завершить в 2020 году.
По состоянию на 27 сентября 2018 года 21 из 22 (95 процентов) пациентов были бессобытийно живы (прим. «событие» смерть или необходимость в длительной вентиляции легких более 16 часов в сутки). Средний возраст составлял 9,5 месяцев, 6 из 7 (86 процентов) пациентов смогли достичь возраста в 10,5 месяцов или старше без событий на указанную дату. Естественная история развития заболевания без лечения показывает, что 50 процентов детей с СМА 1-го типа не выживут или будут нуждаться в постоянной вентиляции к возрасту 10,5 месяцев.
Оценки по шкале специального теста нервно-мышечных расстройств CHOP-INTEND увеличились в среднем на 7,0 баллов через месяц после применения терапии и на 11,8 баллов через три месяца, отражая улучшение двигательной функции по сравнению с исходным уровнем.
Эти данные сопоставимы с улучшениями CHOP-INTENDпри предложенной терапевтической дозе когорты (2-я когорта) в основном исследовании START, которое продемонстрировало среднее соответственное увеличение на 9,8 и 15,4 баллов на том же отрезке времени. Раннее увеличение баллов по CHOP-INTENDможет быть связано с возможным достижением моторных навыков пациентами.
Предварительные оценки пациентов, получавших Zolgensma, показали улучшение двигательных навыков. Три пациента могли сидеть без поддержки в течение не менее 30 секунд по состоянию на 27 сентября 2018 года (медиана возраста — 9,4 месяца) и восемь пациентов достигли того же рубежа к 31 декабря 2018 года (средний возраст — 12,5 месяцев).
| контрольная отметка, кол-во пациентов n (%) | 3 фаза исследования STR1VE, n=22 | |
| 27 сентября 2018 | 31 декабря 2018 | |
| Держит голову прямо 3 и более секунд без поддержки | 12 (54,5) | 17 (77,3) |
| Переворачивается со спины и в правую, и в левую стороны | 3 (13,6) | 7 (31,8) |
| Сидит без поддержки 30 и более секунд | 3 (13,6) | 8 (36,4) |
| Стоит с помощью | 1 (4,5) | |
| Средняя продолжительность наблюдения при сборе данных | 5,5 месяцев | 8,1 месяцев |
| Средний возраст при сборе даных | 9,4 месяцев | 12,5 месяцев |
| Пациенты старше 12 месяцев, кол-во n (%) | 5 (22,7) | 13 (59,1) |
Наблюдения за безопасностью сравнимы с наблюдениями в 1-й фазе ключевого исследования START. Неблагоприятные события, представляющие особый интерес, включая повышение уровня трансаминаз, снижение количества тромбоцитов и тромбоцитопения, были преходящими и не вызывали каких-либо долгосрочных последствий. Один пациент умер от дыхательной недостаточности, которая была признана исследователем и независимым советом по мониторингу безопасности данных не связанной с лечением. Этот пациент продемонстрировал значительное улучшение моторики, с увеличением CHOP-INTENDна 27 баллов по сравнению с исходным уровнем через пять месяцев после вливания.
AveXis благодарен мужественным пациентам и семьям, которые принимают участие в наших испытаниях, что позволяет нам продолжать прилагать усилия по осуществлению значительных изменений в жизнь пациентов с редкими генетические заболеваниями.
Причины
Как было сказано ранее, болезнь передается по наследству, и основные причины развития — генетические мутации. В результате чего прекращается выработка специального белка, отвечающего за функционирование двигательных нейронов. Таким образом, те нейроны, которые успели сформироваться и начать свою полноценную деятельность разрушаются, а это приводит к невозможности передачи нервных импульсов и как результат нарушение или полное отсутствие контроля за мышцами.
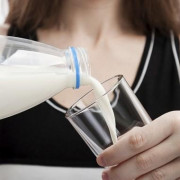
Для формирования болезни необходимо, чтобы мать и отец были носителями неправильного гена. В таком случае атрофия мышечная развивается у ребенка с вероятностью 25%.
Биохимические исследования
При амиотрофии установлено умеренное повышение активности ферментов: альдолазы, креатинфосфокиназы, трансаминаз в сыворотке крови. Однако по сравнению с первичными миопатиями (см.) это повышение выражено значительно слабее. Другим характерным биохимическим признаком амиотрофии является креатинурия, отражающая степень атрофии мышечной ткани; одновременно у больных снижается экскреция с мочой креатинина. Креатининовый показатель мочи, представляющий отношение креатинина к сумме креатина и креатинина и в норме равный единице, снижается до 0,8 (С. Н. Давиденков). Содержание в плазме крови и в моче у больных амиотрофией свободных аминокислот существенно не меняется. Наследственные амиотрофии следует дифференцировать с мышечными атрофиями (см. Атрофия мышечная). Прогноз неблагоприятный при ранних и быстротекущих формах амиотрофии — больные погибают в детском возрасте. При поздних и медленно текущих формах прогноз относительно благоприятный: больные благодаря сохранным мышечным группам могут компенсировать функцию пораженных мышц. Следует избегать переохлаждения и переутомления, ведущих к обострению заболевания.
Родителям, имеющим ребенка, больного спинальной или невральной амиотрофией, рекомендуется воздержание от дальнейшего деторождения.
Диагностика
Наиболее точным методом определения спинально-мышечной атрофии у детей является анализ ДНК. Он проводится как у родившегося малыша, так и во время внутриутробного развития. Дополнительно проводятся следующие исследования:
- Анализ на биохимию. Целью является выяснение уровня ферментов: ананинаминотрансферазы, лактатдегидрогеназы, креатинкиназы. Нормальное их содержание позволяет исключить подозрения на прогрессирующую дистрофию мышц.
- Электрофизиологическое исследование. Метод направлен на регистрацию биоэлектрической активности. Патологию характеризует ритм «частокола».
- МРТ. Назначается для обнаружения признаков атрофии мышц.
- Микроскопия спинного мозга. Отмечаются признаки дегенеративных процессов в клетках нервных отростков. Они сморщиваются, разбухают, при этом глиальные волокна имеют плотную структуру.
- Тандемная масс-спектрометрия. Исследование помогает уточнить уровень аминокислот и белка СМН.
- Гистологическое исследование поперечнополосатых мышц. По результатам будут видны группы мелких волокон.

Если у молодых людей, планирующих рождение ребенка, есть родственники с патологией СМА, им рекомендовано пройти генетическую экспертизу.
Как диагностируют данную патологию?
Екатерина Мартынова, мама Артёма
— Мы молодая семья из Воронежа, в мае мне будет 25 лет, а супругу 26. У нас было много планов, другие приоритеты. Но всё поменялось, когда Артёму, нашему единственному ребёнку, исполнилось 11 месяцев и мы узнали о его диагнозе. Речь идёт о начале 2019 года, тогда в мире была зарегистрирована только «Спинраза».
Мы записались в программу раннего доступа к «Спинразе» и получили таким образом шесть уколов. После первых четырёх инъекций Артём перестал слабеть, начали возвращаться навыки переворота на живот, на бок, стал громче кричать, начал сидеть. Курс закончили в мае 2020 года. Если бы мы не получили «Спинразу», то было бы очень страшно.
В мае 2019 в мире зарегистрировали «Золгенсму». Мы, конечно, осознавали, что такую сумму тем более невозможно собрать. Но потом стали встречать истории, когда это всё же удавалось: на Диму Тишунина, на Матвея Чепуштанова. И тоже решили попробовать.
Деньги собирали на протяжении полугода. До начала пандемии COVID-19 успели провести флешмоб, ярмарку на Масленицу, концерт в поддержку сына. Об Артёме говорили на всех городских праздниках, после этого сбор на сутки ускорялся.
Последние три месяца сбора мы сидели дома и работали через соцсети и звонки. Мы волновались, что всё затихнет на карантине, но на самом деле нам пандемия помогла: люди больше времени проводили в интернете и там узнавали об Артёме. Сбор мы закрыли своими силами, без перевода от какого-то одного человека, но нам помогали крупные организации. Например, один из банков перевёл около 12 млн.
Укол «Золгенсмы» Артём получил 30 июня 2020 года, в два года и два дня. Это не наша вина: дистрибьютора задержали с поставкой. Но врач в НИКИ педиатрии им. Вельтищева пошёл нам навстречу, всё-таки два дня — не критичная разница, тут важнее ориентироваться на вес ребёнка. Препарат ввели за час, первое время поднялась температура, но, как объяснили врачи, это обычное явление. Через две недели всё прошло, а через месяц анализы пришли в норму.
Сейчас Артёму два года и восемь месяцев. Он чувствует себя хорошо, крепнет, становится сильнее. Он, конечно, не побежал, не встал, но ползает с поднятой головой, отталкивается ручками и ножками, поднимает корпус. Это для кого-то мелочь, но для нас — прогресс семимильными шагами. «Золгенсма» работает, и это чудо. В Воронеже ходим в бассейн и на ЛФК, скоро полетим в Тюмень делать ортезы.
Наш сын — настоящий герой. Требовательный мальчик, целеустремлённый, шустрый, энергичный, хотя нам это пока не на руку, потому что концентрация на нуле, а нам нужно терпение. Он добрый, сильный, нежный, ласковый, харизматичный. Когда вырастет, будет непростым человеком, как мне кажется.
Болезнь Артёма сильно изменила нас с мужем. Поменялись приоритеты, мы начали понимать, что в этой жизни ценно. Эта ситуация сплотила нашу семью, мы стали больше друг друга ценить, между нами появилась особенная связь. Я сейчас получаю высшее образование, в этом году у меня диплом. На работу не вернусь, но ищу занятие, чтобы можно было совмещать с семьёй. Папа наш предприниматель, амбициозный, теперь у него ещё больше стимула работать. И, конечно, мы помогаем и продолжим помогать другим деткам. Необходимость тратить свои силы и энергию на это я особенно ясно поняла за время сбора. Чем больше отдаём, тем больше приходит
Важно делать это бескорыстно и не ждать чего-то взамен
Диагностика и лечение болезни Верднига-Хофмана
На ранних стадиях заболевания бывает трудно дифференциировать заболевание, так как симптоматика может быть схожа с другими болезнями:
- острый полиомиелит отличается отсутствием прогрессирования заболевания и несимметричными параличами;
- миопатия – также имеет наследственное происхождение, имеет прогрессивное течение, но причиной слабости мышц является нарушение в них обменных процессов;
- врожденная миатония наиболее схожа с болезнью Верднига-Хоффмана, отличить их достаточно можно с помощью биопсии мышечной ткани.
Для диагностики заболевания неврологу понадобятся данные о первом проявлении симптомов, характере их развития, наличия сопутствующих заболеваний.
Проводится ряд исследований для постановки диагноза:
- Электронейромиография выявляет нарушения в работе нервно-мышечной системы. Наблюдаются изменения по мышечному типу, что указывает на патологию двигательного нейтрона;
- Генетический анализ выявляет мутацию гена SMN;
- Биохимия крови на уровень креатинкиназы, показатели в пределах нормы не исключают заболевание;
- Биопсия мышц для морфологического исследования, которое выявляет пучковую атрофию мышечных волокон, чередующихся со здоровыми, а также разрастание соединительной ткани;
- МРТ для исключения других заболеваний.
Для проведения диагностики плода внутриутробно применяется метод биопсии хориона, кордоцентез, амниоцентез. Выявление заболевания является показанием к прерыванию беременности. Вылечить пациента с болезнью Верднига-Хоффмана невозможно. Для продления жизни и улучшения ее качества применяют симптоматическое лечение. Развитие болезни и ухудшение симптомов сдерживают путем обеспечения работы обменных процессов в мышечной ткани.
С помощью лечебной физкультуры и массажа улучшается кровообращение, снижается риск застоев, поддерживается работоспособность мышц, предотвращается неподвижность суставов и потеря ими эластичности. Нагрузки должны быть непродолжительными и осторожными. Физиотерапия способствует удержанию двигательных навыков на имеющемся уровне, их укрепление. Специальные приспособления помогут самостоятельно передвигаться, пользоваться компьютером и даже писать. Портативные аппараты ИВЛ дают возможность пациентам находиться за пределами стационара и проживать жизнь продуктивнее.
Симптомы заболевания
Диета при спинальной амиотрофии
На данный момент еще не подтверждено, что какая-либо диета приносит пользу при СМА.
По мнению большого количества родителей, диета, включающая в себя много белка или специальные добавки к пище, могут повысить силу мышц ребенка. Но, несмотря на очевидную необходимость хорошего питания для больного ребенка, еще не доказано, что ему нужен именно определенный рацион. Причем некоторые продукты даже могут нанести вред его организму.
К примеру, аминокислотное меню порой чревато еще большими проблемами у тех детей, у которых в организме слишком мало мышечной ткани. По мнению некоторых специалистов, при недостатке мышечной ткани, та не может правильно перерабатывать аминокислоты и тогда их уровень в крови повышается слишком сильно.

Некоторым детям полезнее питаться понемногу, причем чаще трех-четырех раз в день. Нужно просто разделить для больного все количество пищи, принимаемое здоровым сверстником больного за день, на несколько частей.
Среди больных СМА есть обладатели лишнего веса. Возможно, что причина этого кроется в слишком калорийном рационе вкупе с недостатком движения. Если есть возможность, больной должен, заручившись помощью врача и диетолога, привести свой вес в норму
Это важно не только для здоровья и внешности, но и для тех, кто ухаживает за таким больным. Ведь они каждый день помогают больному подниматься и перемещаться
Симптомы у ребёнка и взрослого
Основным признаком болезни СМА является мышечная вялость, слабость и атрофия. Однако у каждой из форм спинальных амиотрофий существуют свои особенности:
- При заболевании Вердинга — Гоффмана первые симптомы могут быть обнаружены ещё во время беременности на УЗИ осмотре, так как плод очень слабо шевелится. После родов отмечается невозможность ребёнка самостоятельно держать голову, переворачиваться и позднее сидеть. Почти всё время малыш лежит в расслабленной позе на спине, не имея возможности свести ноги и руки. Также отмечаются частые проблемы с кормлением, так как младенец испытывает трудности с глотанием. Дыхание зачастую нарушено из-за атрофии рёберной мускулатуры. Практически 70% детей погибают, не дожив до двух лет. После диагностики выявляется недостаточная сформированность передних рогов спинного мозга. Если пациент доживает до 7–10 лет, то у него нарастает выраженность мышечной атрофии и он погибает от острой сердечной, лёгочной недостаточности или из-за проблем с пищеварением. В редких случаях больные доживают до 30 лет, и то исключительно при более позднем начале проявления симптомов (около 2 лет).
- При втором типе спинальной мышечной атрофии ребёнок зачастую может самостоятельно дышать и глотать пищу. Однако со временем происходит прогрессирование процесса, и в более старшем возрасте дети оказываются прикованными к инвалидным креслам. Обычно родители начинают замечать, что ребёнок часто спотыкается, падает и у него подгибаются колени. Постепенная невозможность самостоятельно проглатывать пищу появляется с возрастом. Также по мере взросления начинает проявляться сильно выраженное искривление позвоночника (сколиоз). Эта форма считается относительно доброкачественной и позволяет пациентам прожить до старости. В некоторых случаях женщины даже могут выносить и родить ребёнка, однако велик шанс передачи болезни по наследству. При правильном уходе и благодаря регулярным занятиям лечебной физкультурой пациенты могут очень долгое время сохранять дееспособность.
- Ювенильная амиотрофия Кюгельберга — Веландера может впервые регистрироваться в возрасте от двух до восемнадцати лет. На самом раннем этапе симптомы могут отсутствовать, ребёнок полноценно развивается. Постепенно начинает появляться слабость в проксимальных отделах тела, чаще всего в плечах и предплечье. В течение многих лет пациент способен самостоятельно передвигаться и обслуживать себя. Часто наблюдаются мышечные подёргивания (фасцикуляции). Основной пик проявления симптомов регистрируется в возрасте от двух до пяти лет, когда ребёнку вдруг становится сложно бегать, вставать с кровати и подниматься по лестнице. Течение болезни относительно доброкачественное, так как пациент может длительно сохранять возможность самостоятельно передвигаться.
- Бульбоспинальная мышечная атрофия Кеннеди — заболевание, сцепленное с полом, передаётся с Х хромосомой и проявляется исключительно у мужчин во взрослом возрасте. Прогрессирует болезнь медленно и начинается со слабости в мышцах бёдер, затем через 10–15 лет постепенно присоединяются бульбарные расстройства (поражения черепных нервов: языкоглоточного, блуждающего и подъязычного). Так как течение заболевания крайне медленное, то важные функции практически не успевают нарушаться и продолжительность жизни сильно не сокращается. Очень часто болезнь сопровождается эндокринными патологиями: атрофией яичек, снижением либидо, сахарным диабетом.
- Дистальная СМА Дюшена — Арана обычно регистрируется в возрасте 18–20 лет. Первыми поражаются кисти рук, затем полностью верхние конечности. В течение длительного времени постепенно наступает атрофия мышц ног. В крайне редких случаях заболевание останавливается на парезе одной из рук.
- Скапуло-перонеальная спинально-мышечная атрофия Вюльпиана впервые дает о себе знать в старшем возрасте (20–40 лет). Проявляется постепенной атрофией мышц плечевого пояса и разгибателей стопы и голени. Прогноз относительно благоприятный, так как, даже спустя 30 лет с момента начала заболевания, у пациента сохраняется возможность передвигаться самостоятельно.
СМА у беременных связана со множеством осложнений. Зачастую самостоятельно родить женщина не может и ей назначают кесарево сечение.
На рентгеновских снимках видно искривление позвоночника и последующее его исправление с помощью операции
Лечение
К сожалению, на сегодняшний день медицинская наука не может предложить методов и средств для лечения СМА. Таких методов не существует. Для поддержания функций организма и максимального продления периода, пока ребенок может двигаться сам, рекомендуются такие медикаменты, как «Прозерин», «Оксазил». Они снижают активность фермента, способного расщеплять ацетилхолин, передающий импульс возбуждения по волокнам нервной системы.
Также рекомендуется систематический прием средств, усиливающих энергообмен на клеточном уровне, витаминов группы В, ноотропных средств, а также препаратов калия и никотиновой кислоты.
Ребенку с СМА показано соблюдение диеты с высоким содержанием белка, но последние исследования показали, что роль диеты несколько преувеличена – нет доказательств, что большое содержание протеина в пище хоть каким-то образом влияет на скорость прогрессирования недуга.
Помочь продлить период более-менее полноценной жизни помогут лечебный массаж, УВЧ, электрофорез, программы дыхательной гимнастики для поддержания дыхательных мышц, плавание. Рекомендуется ношение поддерживающих спинных и грудных ортопедических приспособлений.
Подробнее о болезни рассказывает специалист в видео, представленном ниже.
Помогающие организации
Благотворительный фонд «Семьи СМА» — единственная в России организация, специализирующаяся на помощи семьям, столкнувшимся со спинальной мышечной атрофией. Оказывается благотворительную, информационную, психологическую поддержку семьям, консультирует специалистов по вопросам заболевания и методов работы с пациентами со СМА.
Фонд помощи хосписам «Вера». Благотворительная и консультативная помощь семьям с неизлечимо больными детьми, неизлечимо больным взрослым.
ОДКБ № 1 Отделение паллиативной помощи детям, Екатеринбург, Свердловская область. Оказывается медицинскую, информационную, социальную и психологическую помощь семьям, воспитывающим ребенка-инвалида с паллиативным состоянием.
«Научно-исследовательский клинический институт педиатрии имени академика Ю.Е. Вельтищева» ФГБОУ ВО РНИМУ им.Н.И.Пирогова. Институт находится в Москве. Обращаться за медицинской помощью детям со СМА и другими нервно-мышечными заболеваниями могут жители всей России.
Клиника «Чайка». Консультации врача-пульмонолога Штабницкого Василия Андреевича для детей и взрослых со СМА.
Детский хоспис «Дом с маяком» (Москва, ближнее Подмосковье). Медицинская, психологическая, правовая, социальная, благотворительная помощь семьям с неизлечимо больными детьми и молодыми взрослыми (до 25 лет).
Марфо-Мариинский медицинский центр «Милосердие» (г.Москва). Медицинская, психологическая, правовая помощь, помощь няни, мероприятия, духовная поддержка, благотворительная помощь семьям с неизлечимо больными детьми.
Более подробную информацию вы найдете на сайте благотворительного фонда «Семьи СМА» и их специального проекта о жизни со спинальной мышечной атрофией
Спецпроект предназначен тем, кто столкнулся с диагнозом СМА и хотел бы узнать все самое важное об этой болезни: к каким специалистам и куда обращаться, как ухаживать, за чем следить, о чем помнить, какая терапия существует на сегодняшний день.