Американский трипаносомоз (болезнь шагаса)
Содержание:
- Эпидемиология
- Эпидемиология
- Деятельность ВОЗ
- Другие заболевания из группы Инфекционные и паразитарные болезни:
- Online-консультации врачей
- Лечение
- Жизненный цикл
- Жизненный цикл
- Диагностика Болезни Шагаса (американского трипаносомоза):
- Особенности трихомоноза у девочек
- Клиническая картина
- Этиология
- Профилактика Болезни Шагаса (американского трипаносомоза):
Эпидемиология
Основным источником Т. gambiense является человек (больной или паразитоноситель), однако паразита находили также у свиней, коров, овец. Переносчиками Т. gambiense являются мухи цеце группы paipalis (Glossina paipalis, G. tachinoides, G. fuscipes и др.), к-рые питаются на людях, а также на домашних животных. На основании этого допускается, что дополнительным источником инвазии может быть домашний скот. Мухи группы palpalis обитают на территориях Центральной и Западной Африки, отличающихся повышенной влажностью, гл. обр. в лесах и в густых зарослях по долинам рек. Мухи нападают днем, зараженность их трипаносомами обычно невелика (ок. 1%). Контакт мух с людьми и домашним скотом резко возрастает в засушливые сезоны, когда число и площадь водоемов уменьшается, люди и животные концентрируются около оставшихся водоемов. В такие периоды интенсивность передачи возбудителей в очагах возрастает, возможны эпидемические вспышки. Болеют преимущественно сельские жители. Часть инвазированных лиц остается паразитоносителями (см. Носительство возбудителей инфекции). Эндемичные по гамбийскому трипаносомозу территории имеют тенденцию уменьшаться под влиянием деятельности человека, однако все местности, заселенные мухами цеце, должны рассматриваться как потенциально эпидемически опасные.
Источник инвазии Т. rhodesien-se — антилопы, возможно, другие дикие животные и человек. Переносчиками возбудителя являются мухи цеце группы morsitans (G. morsi-tans, G. pallidipes, G. swynnertoni и др.). Их биотопами являются кустарниковые заросли восточноафриканских саванн и чащи по берегам озер, основными «прокормителями» — дикие животные (антилопы, дикие кабаны и др.). Родезийский трипаносомоз — природно-очаговая инвазия. Люди подвергаются нападению мух цеце и заражаются Т. rho-desiense при посещении природного очага с целью охоты, рыбной ловли. В селениях очаги С.б. возникают при большой численности мух G. morsitans. Передача возбудителей в этих случаях происходит по цепи больной человек — муха — человек.
Эпидемиология
Африканский трипаносомоз
Переносчиками трипаносом служат кровососущие мухи цеце. Развитие личинок и куколок происходит в умеренновлажных и затененных местах почвы. Мухи цеце питаются кровью человека и животных. В организме насекомых трипаносома проходит цикл развития длительностью около 20 дней, завершающийся образованием инвазионных (заразных) метациклических форм трипомастигот. Инвазионные мухи передают трипаносомы человеку в процессе кровососания в течение всей жизни, продолжительность которой составляет несколько месяцев. Одного укуса инфицированной мухой цеце достаточно для развития заболевания, так как она выделяет со слюной за один укус до 40 тыс. трипаносом. Возможна передача инфекции при гемотрансфузиях (переливаниях крови носителей трипаносом здоровым людям).
Гамбийская форма африканского трипаносомоза относится к антропонозам (инфекциям, передающимся от человека к человеку); дополнительным носителем и источником инфекции, возможно, служат свиньи. Переносчики возбудителя обитают в так называемых галерейных лесах и зарослях по берегам рек и ручьев. Заболевание распространено в странах Западной и Центральной Африки. Заболеваемость может принимать характер эпидемических вспышек, чаще всего в сухой сезон года.
Родезийская (восточноафриканская) форма африканского трипаносомоза — зоонозная природно-очаговая инвазия. Основным резервуаром служат лесная антилопа, другие дикие животные, иногда крупный рогатый скот. Заболевание распространено в саваннах Восточной и Южной Африки. Заражение людей происходит главным образом во время пребывания на территории природных очагов. Обычно родезийская форма трипаносомоза регистрируется в виде единичных случаев, но отмечены и эпидемические вспышки. Чаще болеют мужчины. В последние годы описаны вспышки трипаносомоза, вызванного паразитом животных, среди населения Эфиопии. Возможен завоз африканского трипаносомоза в Россию.
Американский трипаносомоз
Основными переносчиками возбудителей американского трипаносомоза являются клопы. Заражение клопов происходит при питании кровью человека или животных, содержащей трипомастиготы. Через 10—30 дней в прямой кишке клопа появляются инвазионные (заразные) трипомастиготы, выделяемые с экскрементами наружу. Будучи однократно инвазированными, клопы сохраняют трипаносом в течение всей своей жизни (около 2 лет). Трипаносомы проникают в организм человека или животных во время укуса с фекалиями клопов. Возможны также алиментарный путь заражения (с пищевыми продуктами) и передача инфекции при гемотрансфузиях. Инфекция может распространяться и вертикально (через плаценту). Известны синантропные (расположенные вблизи человеческого жилья) и природные очаги болезни Чагаса. В очагах первого типа клопы обитают в глинобитных домах, хлевах, птичниках, норах домовых грызунов. В этих очагах, кроме человека, носителями возбудителя являются собаки, кошки, свиньи и другие домашние животные. В природных очагах резервуарами возбудителя служат броненосцы, муравьеды, лисы, обезьяны и др.
Заражение людей происходит в теплое время года при посещении этих очагов, когда максимально активны переносчики. Чаще заражаются мужчины. Болезнь Чагаса регистрируется в течение всего года во всех возрастных группах, но чаще у детей. Более характерны единичные случаи, но при массовом нападении триатомовых клопов на людей возможны эпидемические вспышки. Болезнь Чагаса широко распространена, она выявляется практически во всех странах Американского континента, особенно значительные очаги расположены в латиноамериканских странах к югу от Мексики. Наиболее часто случаи болезни регистрируются в Бразилии, Аргентине, Венесуэле. В других частях света инфекция не встречается.
Деятельность ВОЗ
ВОЗ оказывает содействие и техническую поддержку национальным программам по борьбе с сонной болезнью.
Она бесплатно предоставляет эндемичным странам противотрипаносомные лекарственные средства в рамках публично-частных партнерств с компаниями Sanofi (пентамидин, меларсопрол, эфлорнитин и фексинидазол) и Bayer HealthCare (сурамин и нифуртимокс). Подготовка и грузоперевозка лекарств осуществляется совместно с логистическими специалистами организации «Врачи без границ».
Для упрощения разработки новых и доступных по стоимости диагностических средств ВОЗ в 2009 г. создала банк образцов биоматериалов, которыми могут пользоваться исследователи. В банке хранятся образцы крови, сыворотки, спинномозговой жидкости, слюны и мочи, взятые у пациентов, инфицированных обеими формами болезни, а также образцы, взятые у неинфицированных людей из эндемичных районов.
В 2008 г. ВОЗ выступила с инициативой по созданию атласа африканского трипаносомоза человека с данными обо всех зарегистрированных случаях заболевания на уровне сельских населенных пунктов. Эта инициатива осуществляется совместно с ФАО в рамках Программы борьбы с африканским трипаносомозом (ПБАТ). Атлас представляет собой динамичную базу данных, включающую географические и эпидемиологические данные, собранные ВОЗ на основе информации, представляемой национальными программами по борьбе с сонной болезнью, НПО и научно-исследовательскими институтами.
В 2014 г. в целях активизации и поддержки усилий по элиминации болезни по инициативе ВОЗ была создана координационная сеть по африканскому трипаносомозу человека. В число заинтересованных партнеров этой сети вошли национальные программы по борьбе с сонной болезнью, организации, занимающиеся поиском новых средств по противодействию ей, международные и неправительственные организации, а также доноры.
Программа ВОЗ призвана решать следующие задачи:
- усиление и координация мер борьбы с болезнью и обеспечение стабильной деятельности на местах;
- укрепление систем эпиднадзора;
- обеспечение доступа к услугам диагностики и наиболее эффективным лекарственным средствам;
- содействие мониторингу эффективности лечения и тенденций возникновения лекарственной устойчивости;
- ведение информационной базы данных для целей эпидемиологического анализа, в том числе атласа африканского трипаносомоза человека, разработанного в сотрудничестве с Продовольственной и сельскохозяйственной организацией ООН (ФАО);
- организация мероприятий по подготовке квалифицированного персонала;
- поддержка операционных исследований, направленных на совершенствование средств диагностики и лечения;
- расширение сотрудничества с ФАО, занимающейся вопросами трипаносомоза животных, и Международным агентством по атомной энергии (МАГАТЭ), занимающимся вопросами борьбы с переносчиками путем радиационной половой стерилизации самцов мух. Эти три учреждения ООН вместе с Африканским союзом содействуют осуществлению Программы борьбы с африканским трипаносомозом (ПБАТ);
- обеспечение согласованности мероприятий по борьбе с переносчиками и противодействию болезни в сотрудничестве с Панафриканской кампанией Африканского союза по ликвидации цеце и трипаносомоза (PATTEC).
Другие заболевания из группы Инфекционные и паразитарные болезни:
| Абдоминальный актиномикоз |
| Аденовирусная инфекция |
| Аденовирусный энтерит |
| Акантохейлонематоз (дипеталонематоз) |
| Актиномикоз |
| Амебиаз |
| Амебный абсцесс легкого |
| Амебный абсцесс печени |
| Анизакидоз |
| Анкилостомидоз |
| Анкилостомоз |
| Аргентинская геморрагическая лихорадка |
| Аскаридоз |
| Аспергиллез |
| Бабезиоз |
| Балантидиаз |
| Бартонеллез |
| Беджель |
| Бешенство |
| Бластомикоз Гилкриста |
| Бластомикоз южно-американский |
| Болезнь (лихорадка) Росс-Ривер |
| Болезнь Брилла-Цинссера |
| Болезнь кошачьих царапин |
| Болезнь Кройцфельдта-Якоба |
| Болезнь Лайма |
| Болезнь Шагаса (американский трипаносомоз) |
| Боливианская геморрагическая лихорадка |
| Ботулизм |
| Бразильская пурпурная лихорадка |
| Бругиоз |
| Бруцеллёз |
| Брюшной тиф |
| Ветряная оспа (ветрянка) |
| Вирусные бородавки |
| Вирусный гепатит A |
| Вирусный гепатит В |
| Вирусный гепатит Е |
| Вирусный гепатит С |
| Вирусный конъюнктивит |
| Висцеральный лейшманиоз |
| Внезапная экзантема |
| Возвратный тиф |
| Вухерериоз (слоновая болезнь) |
| Газовая гангрена |
| Геморрагическая лихорадка с почечным синдромом |
| Геморрагическая лихорадка Эбола |
| Геморрагические лихорадки |
| Гемофильная инфекция |
| Герпетическая ангина (герпетический тонзиллит) |
| Герпетическая экзема |
| Герпетический менингит |
| Герпетический фарингит |
| Гименолепидоз |
| Гирудиноз |
| Гистоплазмоз легких |
| Гнатостомоз |
| Головной педикулёз |
| Грипп |
| Дикроцелиоз |
| Дипилидиоз |
| Дифиллоботриоз |
| Дифтерия |
| Дракункулёз |
| Жёлтая лихорадка |
| Зигомикоз (фикомикоз) |
| Иерсиниоз и псевдотуберкулез |
| Изоспороз |
| Инфекционная эритема (пятая болезнь) |
| Инфекционный мононуклеоз |
| Кампилобактериоз |
| Капилляриоз кишечника |
| Капилляриоз легочный |
| Капилляриоз печеночный |
| Кишечный интеркалатный шистосомоз |
| Кишечный шистосомоз Мэнсона |
| Клонорхоз |
| Кожно-слизистый лейшманиоз (эспундия) |
| Кожный лейшманиоз |
| Кожный миаз |
| Коклюш |
| Кокцидиоидомикоз |
| Колорадская клещевая лихорадка |
| Контагиозный моллюск |
| Корь |
| Краснуха |
| Криптококкоз |
| Криптоспоридиоз |
| Крымская геморрагическая лихорадка |
| Ку-лихорадка |
| Кьясанурская лесная болезнь |
| Легионеллёз (Болезнь легионеров) |
| Лейшманиоз |
| Лепра |
| Лептоспироз |
| Листериоз |
| Лихорадка Денге |
| Лихорадка Западного Нила |
| Лихорадка Ласса |
| Лихорадка Марбург |
| Лихорадка от укуса крыс (Содоку) |
| Лихорадка Рифт-Валли |
| Лихорадка Чикунгунья |
| Лоаоз |
| Лобковый педикулез |
| Лобомикоз |
| Лямблиоз |
| Малярия |
| Мансонеллез |
| Медленные вирусные инфекции |
| Мелиоидоз |
| Менингококковая инфекция |
| Миаз |
| Мицетома |
| Москитная лихорадка (лихорадка паппатачи) |
| Мочеполовой шистосомоз |
| Натуральная оспа |
| Некатороз |
| Нокардиоз |
| Окопная лихорадка |
| Омская геморрагическая лихорадка |
| Онхоцеркоз |
| Описторхоз |
| Опоясывающий лишай (опоясывающий герпес) |
| Оппортунистические микозы |
| ОРВИ |
| Осповидный риккетсиоз |
| Острый герпетический (афтозный) стоматит |
| Острый герпетический гингивостоматит |
| Острый полиомиелит |
| Парагонимоз человека |
| Паракокцидиоидомикоз |
| Паратиф С |
| Паратифы А и В |
| Парвовирусная инфекция |
| Паротитный менингит |
| Паротитный орхит |
| Паротитный панкреатит |
| Паротитный энцефалит (энцефалит при эпидемическом паротите) |
| Пастереллез |
| Педикулёз (вшивость) |
| Педикулёз тела |
| Пенициллоз |
| Пинта |
| Пищевые токсикоинфекции |
| Пневмоцистоз (пневмоцистная пневмония) |
| Простуда |
| Пятнистая лихорадка Скалистых гор |
| Ретровирусная инфекция |
| Рожа |
| Ротавирусный энтерит |
| Сальмонеллез |
| Сап |
| Сибирская язва |
| Синдром токсического шока |
| Синдром Уотерхауза-Фридериксена |
| Скарлатина |
| Спарганоз |
| СПИД (синдром приобретённого иммунного дефицита) |
| Спириллез |
| Споротрихоз |
| Стафилококковое пищевое отравление |
| Столбняк |
| Стрептобациллез |
| Стронгилоидоз |
| Тениоз |
| Токсоплазмоз |
| Трихинеллез |
| Трихостронгилоидоз |
| Трихоцефалёз (трихуроз) |
| Тропическая легочная эозинофилия |
| Туберкулез периферических лимфатических узлов |
| Туляремия |
| Тунгиоз |
| Фасциолез |
| Фасциолопсидоз |
| Филяриатоз (филяриоз) |
| Филяриатоз лимфатический |
| Фрамбезия |
| Холера |
| Хромомикоз |
| Хронический вирусный гепатит |
| Цистицеркоз |
| Цистицеркоз глаз |
| Цистицеркоз головного мозга |
| Цитомегаловирусная инфекция |
| Цитомегаловирусная пневмония |
| Цитомегаловирусный гепатит |
| Цитомегаловирусный мононуклеоз |
| Чесотка |
| Чума |
| Шейно-лицевой актиномикоз |
| Шигеллез |
| Шистосоматидный дерматит |
| Шистосомоз (бильгарциоз) |
| Шистосомоз японский |
| Энтеробиоз |
| Энтеровирусная инфекция |
| Эпидемическая миалгия |
| Эпидемический паротит (свинка) |
| Эпидемический сыпной тиф |
| Эризипелоид |
| Эхинококкоз |
| Эхинококкоз легких |
| Эхинококкоз печени |
| Эшерихиоз |
| Язвенно-некротический стоматит Венсана |
Online-консультации врачей
| Консультация ортопеда-травматолога |
| Консультация специалиста в области лечения стволовыми клетками |
| Консультация радиолога (диагностика МРТ, КТ) |
| Консультация общих вопросов |
| Консультация педиатра-аллерголога |
| Консультация гинеколога |
| Консультация пульмонолога |
| Консультация нарколога |
| Консультация нейрохирурга |
| Консультация эндоскописта |
| Консультация неонатолога |
| Консультация генетика |
| Консультация оториноларинголога |
| Консультация диетолога-нутрициониста |
| Консультация детского психолога |
Новости медицины
Устройство и принцип работы магнитной мешалки,
26.05.2021
Быстрая доставка лекарств на сервисе mednex.com.ua,
30.04.2021
6 простых привычек, чтобы круглый год не болеть простудами: рекомендуют все врачи,
17.03.2021
Морепродукты становятся вредными для здоровья?,
05.01.2021
Новости здравоохранения
Эксперт назвала три отличия простуды от COVID-19,
05.01.2021
В мире более 86 миллионов случаев COVID-19,
05.01.2021
Скорость распространения COVID-19 зависит от климатических условий,
11.06.2020
Исследователи насчитали шесть разновидностей коронавируса,
11.06.2020
Лечение
Лечение следует проводить как при клин, проявлениях заболевания, так и при трихомонадоноси-тельстве обоим супругам (половым партнерам) одновременно. В период лечения и последующего контроля половая жизнь запрещается. Следует воздействовать на возбудителя, а также на факторы, предрасполагающие к развитию Т.: лечение гиповитаминоза, гипофункции яичников, анемии, сахарного диабета; необходима санация влагалища. Лечение остротекущих форм Т. может ограничиваться одной этиотропной терапией — назначением противотрихомонадных средств.
Из противотрихомонадных средств наибольшее распространение получили трихомонацид (см.), метро-нидазол (см.), фасижин. Лечение метронидазолом проводят преимущественно короткими курсами; его назначают по 0,5 г 2 раза в день во время еды в течение 5 дней. Фасижин дают по 150 мг 2 раза в день в течение 7 дней или однократно 2 000 мг (4 таблетки по 500 мг). Противопоказаниями к приему этих препаратов являются заболевания нервной системы, системы кроветворения, заболевания печени, беременность, лактация и др. Однако в связи с неблагоприятным влиянием Т. на течение беременности (преждевременное прерывание беременности, опасность инфицирования плода, воспалительные процессы в послеродовом периоде) нек-рые врачи рекомендуют применять метронидазол со второго триместра беременности курсами по 4—5 дней в общей дозе 3 г с одновременным назначением местного лечения.
При непереносимости этих препаратов или противопоказаниях к их применению, при рецидивирующем упорном течении заболевания, а также при присоединении канди-доза в результате применения противотрихомонадных средств используют местное лечение. Женщинам назначают канестен в виде р-ра или вагинальных таблеток, р-р натриевой соли леворина, р-р амфоглюка-мина и др. Местное лечение уретрита у мужчин проводят осарсолом в виде порошка или 10% водной или масляной взвеси, к-рую вводят ежедневно в течение 8—10 дней в мочеиспускательный канал. Местное лечение парауретрита заключается в промывании протоков с помощью шприца и иглы с затупленным концом 10% взвесью осарсола. При упорном течении процесса прибегают к облитерирующей терапии или к экстирпации поверхностно расположенного хода. При образовании абсцесса лечение оперативное. Местное лечение баланопостита проводят в течение 10 дней присыпками мет-ронидазола и осарсола после предварительного промывания препуци-ального мешка р-ром антисептика.
Хорошее терапевтическое действие оказывает чередование присыпок с примочками 0,25—0,5% р-ром нитрата серебра.
При простатитах, везикулитах, эпидидимитах, куперитах целесообразно назначать также антибиотики широкого спектра действия.
В ряде случаев после лечения у мужчин остается посттрихомонадный воспалительный процесс, проявляющийся в период контрольного наблюдения скудными непостоянными выделениями. Они связаны с пато-морфол. изменениями в слизистой оболочке мочеполовых органов, с наличием сопутствующей микрофлоры (грибки, стафилококки и др.) при полном исчезновении трихомо-над. Для борьбы с этим воспалением применяют инстилляции в уретру раздражающих химических и антисептических средств, бужирова-ние, введение тампонов и др.
Лица, перенесшие Т., после лечения должны находиться под диспансерным наблюдением.
Критерием излеченности у женщин считаются отрицательные результаты анализов при исследовании материала из различных отделов мочеполовой системы на 1-й, 2-й и 3-й день после окончания менструации в течение трех менструальных циклов. Контрольные исследования у мужчин проводятся через 7—10 дней, 1 мес. и 2 мес. после окончания лечения. Критерием излеченности у мужчин является прекращение выделений из мочеиспускательного канала, а также отсутствие простейших в секрете предстательной железы. Контроль следует проводить лучше после механической и алиментарной провокации.
Прогноз благоприятный при условии проведения комплексного лечения Т. У женщин неизлеченный Т. способствует развитию лейкоплакии (см.) и крауроза вульвы (см.), у мужчин невылеченный трихомонад-ный баланопостит может привести к фимозу (см.) и парафимозу (см.). Двусторонний трихомонадный орхо-эпидидимит в 70—80% случаев является причиной бесплодия.
Профилактика включает меры общественной профилактики (выявление больных Т., их лечение, диспансерное наблюдение), а также личную профилактику (подробно см. Гонорея).
Жизненный цикл
Жизненный цикл Trypanosoma brucei
T. brucei завершает свой жизненный цикл между мухой цеце (из рода Glossina ) и млекопитающими-хозяевами, включая людей, крупный рогатый скот, лошадей и диких животных.
У млекопитающего-хозяина
Заражение происходит, когда муха-переносчик цеце кусает млекопитающего-хозяина. Муха вводит метациклические трипомастиготы в ткань кожи. Трипомастиготы попадают в лимфатическую систему и в кровоток. Начальные трипомастиготы короткие и коренастые. Попадая в кровоток, они вырастают в длинные и тонкие формы. Затем они размножаются за счет двойного деления . Затем дочерние клетки снова становятся короткими и коренастыми. Длинные тонкие формы способны проникать в эндотелий кровеносных сосудов и проникать в внесосудистые ткани, включая центральную нервную систему (ЦНС). Иногда мухой цеце могут заражаться дикие животные, которые действуют как резервуары. У этих животных они не вызывают болезни, но живой паразит может передаваться обратно нормальным хозяевам.
В мухе цеце
Короткие и коренастые трипомастиготы поглощаются мухами цеце во время приема пищи с кровью. Трипомастиготы попадают в среднюю кишку мухи, где становятся проциклическими трипомастиготами. Они быстро делятся и становятся эпимастиготами. Эпимастиготы мигрируют из кишечника через преджелудок в слюнные железы, где они прикрепляются к эпителию слюнных желез. В слюнных железах некоторые паразиты отделяются и превращаются в короткие и коренастые трипомастиготы. Они становятся инфекционными метациклическими трипомастиготами. Они вводятся млекопитающему-хозяину вместе со слюной при укусе. Полное развитие на лету занимает около 20 дней.
В случае T. b. brucei, заражающий G. p. gambiensis , за это время паразит изменяет протеомное содержимое головы мухи. Это может быть причиной наблюдаемых поведенческих изменений, особенно излишне увеличенной частоты кормления, что увеличивает возможности передачи. Это может быть частично связано с наблюдаемым измененным метаболизмом глюкозы , вызывающим предполагаемую потребность в большем количестве калорий. (Метаболические изменения, в свою очередь, происходят из-за полного отсутствия глюкозо-6-фосфат-1-дегидрогеназы у инфицированных мух.) Синтез моноаминовых нейротрансмиттеров также изменяется: производство ароматической декарбоксилазы L-аминокислот, участвующей в синтезе дофамина и серотонина — и индуцировался сверхчувствительный белок α-метилдопа . Это очень похоже на изменения в протеомах головы других двукрылых переносчиков при заражении другими эукариотическими паразитами млекопитающих, обнаруженные в другом исследовании той же группы в том же году.
Жизненный цикл
Все трипаносомы являются паразитическими и подвергаются переключению хозяина между беспозвоночным переносчиком и позвоночным хозяином . У беспозвоночных переносчиков размножение происходит часто, но не во всех случаях; некоторые виды, такие как Trypanosoma evansi , передаются только механически насекомыми без размножения, Trypanosoma equiperdum полностью без насекомого- хозяина во время спаривания от лошади к лошади. Как правило, формы, которые развиваются в кишечном тракте насекомого, — это эпимастигота, а у позвоночного хозяина — трипомастигота. У позвоночных паразиты живут в жидкостях организма, таких как кровь , лимфа или спинномозговая жидкость . Некоторые виды, такие как Trypanosoma cruzi , размножаются в форме амастигот внутри клеток-хозяев, чтобы избежать активности иммунной системы позвоночных- хозяев . Другие трипаносомы, такие как Trypanosoma brucei , разработали сложные механизмы вариабельности антигена , при которых вариабельные поверхностные гликопротеины клеточной оболочки часто обмениваются, чтобы избежать приобретенного иммунитета хозяина.
Диагностика Болезни Шагаса (американского трипаносомоза):
Диагностика болезни Шагаса основана на обнаружении трипаносом у больного или на положительных результатах серологических исследований. В острой фазе болезни трипаносомы могут быть обнаружены в пробах периферической крови теми методами, что и при африканском трипаносомозе. Эффективен микрогематокритный метод обогащения. Если указанные методы не дают положительных результатов, можно провести посевы крови на целый ряд искусственных сред или ввести ее крысам, мышам или морским свинкам.
Возбудители болезни Шагаса хорошо растут в кровяном бульоне при температуре 28°С. В эндемичных районах часто используется метод ксенодиагностики; выращенному в лаборатории свободному от трипаносом переносчику дают напиться крови у больного с подозрением на болезнь Шагаса, и через 2 нед содержимое кишечника насекомого проверяют на наличие возбудителя. Обнаружение трипаносом в крови иногда приводит к путанице. Дело в том, что многие дети в Венесуэле и других странах Южной Америки являются носителями безвредного вида трипаносом (Т. rangeli), который не вызывает болезни, но может находиться в крови в течение многих месяцев.
При повторном применении методов культивирования и ксенодиагностики трипаносомы обнаруживаются у большинства больных в острой фазе и в 40% случаев в хронической фазе инфекции. С помощью биопсии пораженного лимфатического узла или икроножной мышцы возбудителей можно обнаружить в начальном периоде болезни, когда трипаносом не удается выделить из крови. Тест Машад-Гуэррейро (реакция связывания комплемента) наиболее эффективен при диагностике хронических случаев и проведении специальных обследований.
Реакция флюоресцирующих антител и реакция торможения гемагглютинации, по-видимому, более чувствительны, но менее специфичны. Ускоренная реакция агглютинации на предметном стекле была разработана для применения на станциях переливания крови. Во всех этих серологических реакциях используются неочищенные антигены эпимастигот, которые дают перекрестные реакции с сыворотками больных лейшманиозом или с инфекцией, вызванной Т. rangeli. Этих ложноположительных результатов можно избежать, применяя новую иммуноферментную реакцию с использованием очищенного гликопротеидного антигена.
Особенности трихомоноза у девочек
У девочек трихомонадный вуль-вовагинит встречается, как правило, в период новорожденности и полового созревания. В период новорожденности заражение происходит при прохождении плода по инфицированным родовым путям матери. Возможность заражения Т. именно в это время, по мнению многих исследователей, обусловлена тем, что состояние влагалища новорожденной девочки не отличается от такового у взрослой женщины (многослойный плоский эпителий, pH секрета 4,5— 4,0, накопление в эпителии гликогена). У девочек в возрасте от 1 мес. и до начала полового созревания в связи с особенностями состояния влагалища в этот период (однослойный эпителий, нейтральная или щелочная реакция секрета, низкое содержание гликогена, молочной к-ты и др.), при к-рых отсутствуют условия для существования три-хомонад даже в случае их попадания в половые пути, заболевание отмечается чрезвычайно редко. Поэтому при обнаружении трихо-монад в мазках из влагалища девочек необходимы повторное исследование и тщательный сбор анамнеза (выяснение возможного пути заражения). В пубертатном периоде в связи с увеличением концентрации эстрогенов в организме девочки состояние влагалищного эпителия приближается к таковому у взрослых женщин. В этот период у девочек возможно возникновение трихомо-надного кольпита, причем пути заражения и клин, картина не отличаются от таковых у взрослых.
Лечение трихомонадного кольпита у новорожденных заключается в механическом удалении трихомонад с помощью промывания влагалища через тонкий катетер настоями ромашки, шалфея, р-ром фурацилина. Одновременно проводят лечение родителей девочки. При лечении трихомоноза у девочек в пубертатном периоде производят инстилляцию во влагалище 1—3% водного р-ра метиленового синего или после орошения влагалища через тонкий катетер 1 % р-ром гидрокарбоната натрия вводят 1—2 мл 2,5% суспензии нитазола. Кроме того, применяют внутрь указанные выше специфические препараты с учетом возраста и веса (массы) тела ребенка. Осарсол детям не назначают. Ребенок допускается в детский коллектив лишь после получения отрицательных результатов после трехкратного (через день) бактериоскопического исследования. В каждом конкретном случае должен быть решен вопрос о путях заражения.
Библиогр.: Бакшеев Н. С. и Пад-ч е н к о И. К. Мочеполовой трихомоноз у женщин, М., 1971; Б о д я ж и-н а В. И. и Ж м а к и н К. Н. Гинекология, с. 128, М., 1977; Венерические болезни, под ред. О. К. Шапошникова, М., 1980; Гальпровиозы (хламидиозы) человека и животных, под ред. О. В. Барояна, в. 1, с. 5, М., 1979; Ильин И. И., Негонококковые уретриты у мужчин, с. 153, М., 1983; Лазаревич И. П., Паразиты женских половых органов, Харьков, 1870; Ляховицкий H. CU Трихомоноз мужчин, женщин и детей, М., 1966; Овчинников H. М. Лабораторная диагностика венерических заболеваний, М., 1969; П о й з н е р Б. С., Радионченко А. А. и Рыбников В. И. Трихомонадные заболевания женского организма, Томск, 1970; Семенов П. П. и Семенов В. П. Трихомонадные поражения мочеполовых органов человека, Л., 1972; Теохаров Б. А. Гонорея, трихомониаз и другие мочеполовые венерические болезни, М., 1968; он же, Эпидемиология мочеполового трихомоноза у девочек и девушек, Вестн. дерм, и вен., № 2, с. 81, 1978, библиогр.; Тимошенко Л. В. и др. Практическая гинекология, с. 81, Киев, 1980.
Клиническая картина
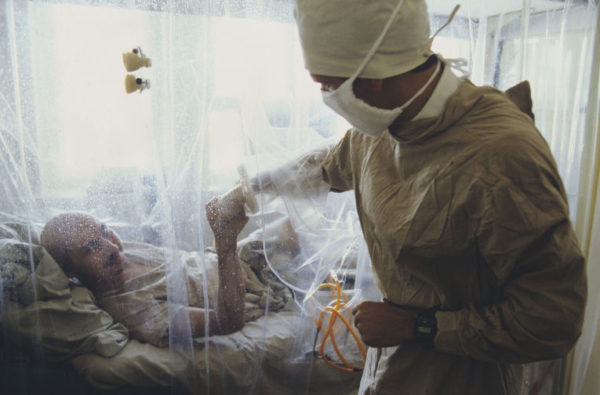
Инкубационный период 5—14 дней. Острая стадия Шагаса болезни наблюдается преимущественно у детей в возрасте от 1 года до 5 лет и взрослых, приезжающих в эндемичные по Шагаса болезни районы. Болезнь начинается с недомогания, озноба, головной боли, мышечных болей. Температура повышается до 39—40°, имеет ремиттирующий или постоянный характер. Образующийся нередко на месте внедрения трипаносом первичный аффект напоминает по внешнему виду фурункул, но никогда не нагнаивается. При внедрении паразита через слизистую оболочку глаза первичный аффект проявляется в виде так называемого симптомокомплекса Романьи: конъюнктивит, отек век, с увеличением регионарных лимфатических узлов. Печень, селезенка и периферические лимфатические узлы увеличены. В крови — лейкоцитоз с лимфомоноцитозом.
Изменения сердца — одно из основных проявлений острой стадии болезни. Границы его расширены, тоны приглушены, иногда выслушивается ритм галопа (см. Галопа ритм). В тяжелых случаях развивается и нарастает сердечная недостаточность. Наиболее тяжелым проявлением острой стадии болезни является менпнгоэнцефалит, почти всегда со смертельным исходом. Из поражений других органов описаны орхит (см.), эпидидимит (см.) и паротит (см.). Острая стадия продолжается 4—5 недель, после чего клинические проявления исчезают, и процесс принимает хроническое течение. Эта стадия Шагаса болезни может протекать без клинических проявлений (латентно) или характеризуется изменениями со стороны сердца. Больные жалуются на одышку, сердцебиение, боли в области сердца. Границы сердца расширены, тоны приглушены, пульс малого наполнения, АД снижено, отмечаются расщепление II тона у верхушки сердца и на легочной артерии, систолический шум у верхушки сердца и у нижнего края грудины, экстрасистолия. Характерны выраженные изменения на ЭКГ в виде нарушений внутрижелудочковой проводимости. Особенно часто наблюдается полная блокада правой ножки пучка Гиса (см. Блокада сердца). Течение хронической стадии Шагаса болезни длительное. Постепенно прогрессирует сердечная недостаточность, приводящая, как правило, к летальному исходу. Описаны также случаи внезапной смерти от острой сердечной недостаточности, причиной которой могут быть фибрилляция желудочков, тромбоэмболия или разрыв аневризмы сердца. Частыми проявлениями Шагаса болезни в хронической стадии бывают изменения пищеварительного тракта с расширением его отделов. При этом возникают боли в животе, нарушение глотания, вздутие живота, запоры.
Диагноз в острой стадии Шагаса болезни ставится на основании данных эпидемиологического анамнеза, клин, картины и лабораторных исследований. Обычно исследуют кровь на наличие трипаносом; при отрицательном результате — материал из первичного аффекта, цереброспинальную жидкость, пунктаты лимфатических узлов, селезенки и костного мозга. В хронической стадии трипаносомы редко обнаруживаются в крови и тканях. Для подтверждения диагноза применяют реакцию связывания комплемента (см.), а также проводят биопробу на белых мышах, вводя им кровь больного с последующим исследованием на трипаносом крови животного.
Этиология
Трипаносомы — возбудители африканского трипаносомоза — проходят сложный цикл развития со сменой хозяев. Часть цикла осуществляется в организме позвоночных хозяев (человек, животные), другая часть — в организме насекомых.
Трипаносомы проходят две стадии развития — стадию трипомастиготы и стадию эпимастиготы. У возбудителя американского трипаносомоза описаны еще две стадии — стадия промастиготы и стадия амастиготы. Трипомастиготы паразитируют только в организме человека и животных, размножаются внеклеточно повторным делением. Эпимастиготы существуют только в организме насекомого. Поступая с кровью в организм мухи цеце (переносчик африканского трипаносомоза), трипаносомы попадают в слюнные протоки и железы, где превращаются в эпимастиготы. Через 2—5 дней эпимастиготы трансформируются в трипомастиготы, и мухи становятся заразными.
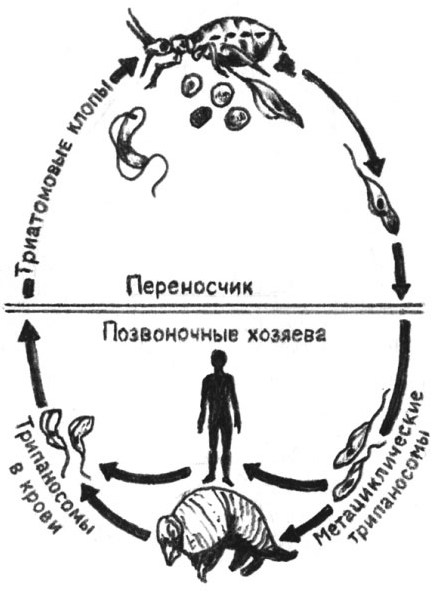
Жизненные циклы трипаносом
Попадая с кровью в организм триатомовых клопов (переносчики американского трипаносомоза), трипаносомы в желудке насекомого превращаются в эпимастиготы и размножаются здесь в течение нескольких дней. Затем они проходят в заднюю и прямую кишку, где возвращаются к трипомастиготной форме. С этого момента клопы становятся заразными. Известны африканский и американский трипаносомозы человека.
Африканский трипаносомоз
Африканский трипаносомоз, или сонная болезнь, — трансмиссивная инфекция, передающаяся через кровососущих переносчиков, в данном случае — муху цеце, характеризующаяся периодами неправильной лихорадки, наличием кожной сыпи, местных отеков и лимфаденитов (см.), развитием кахексии (истощения) и летаргии. Существует в двух формах — гамбийской и родезийской (восточноафриканской), отличающихся по эпидемиологии и особенностям клинического течения. Подробное изучение фаз трипаносомоза в организме мухи цеце было проведено в 1909 г. Второй возбудитель сонной болезни в Африке был описан в 1909—1912 гг.
Американский трипаносомоз
Американский трипаносомоз — болезнь Чагаса. В 1907 г. Чагас обнаружил в кишечнике клопа трипаносому, в 1909 г. он выделил от больного трипаносому, идентичную найденной у клопа. Эти исследования положили начало изучению новой протозойной (вызываемой простейшими) инфекции.
Трипаносома имеет длину 15—20 мкм. В организме человека и млекопитающих животных трипаносомы проникают в клетки внутренних органов и тканей, где превращаются в амастиготы. Со временем амастиготы превращаются в S-образные трипомастиготы, которые поступают в кровь, но в ней не размножаются.
Профилактика Болезни Шагаса (американского трипаносомоза):
Вакцины против болезни Шагаса нет. Профилактика заключается в обработке инсектицидами остаточного действия стен и крыш домов — основных мест обитания переносчиков. При использовании инсектицидов с добавлением латекса образуется бесцветная пленка, которая существенно продлевает активность препарата. Использование фумигантов поможет предупредить повторное появление насекомых. Штукатурение стен, цементирование земляных полов, перенос на большое расстояние от жилых построек штабелей из дров также значительно уменьшают концентрацию переносчиков клопов редувиид в помещениях.
Трансфузионную передачу инфекции можно предупредить, добавляя в препараты крови генциановиолет или его аналоги. В эндемичных районах больных с лейкозом перед началом иммуносупрессивной терапии следует, используя серологические методы, проверить на наличие трипаносомоза.