Факторы, влияющие на сперматогенез
Содержание:
Где образуются сперматозоиды?
Для образования и созревания сперматозоида требуется 72 дня.
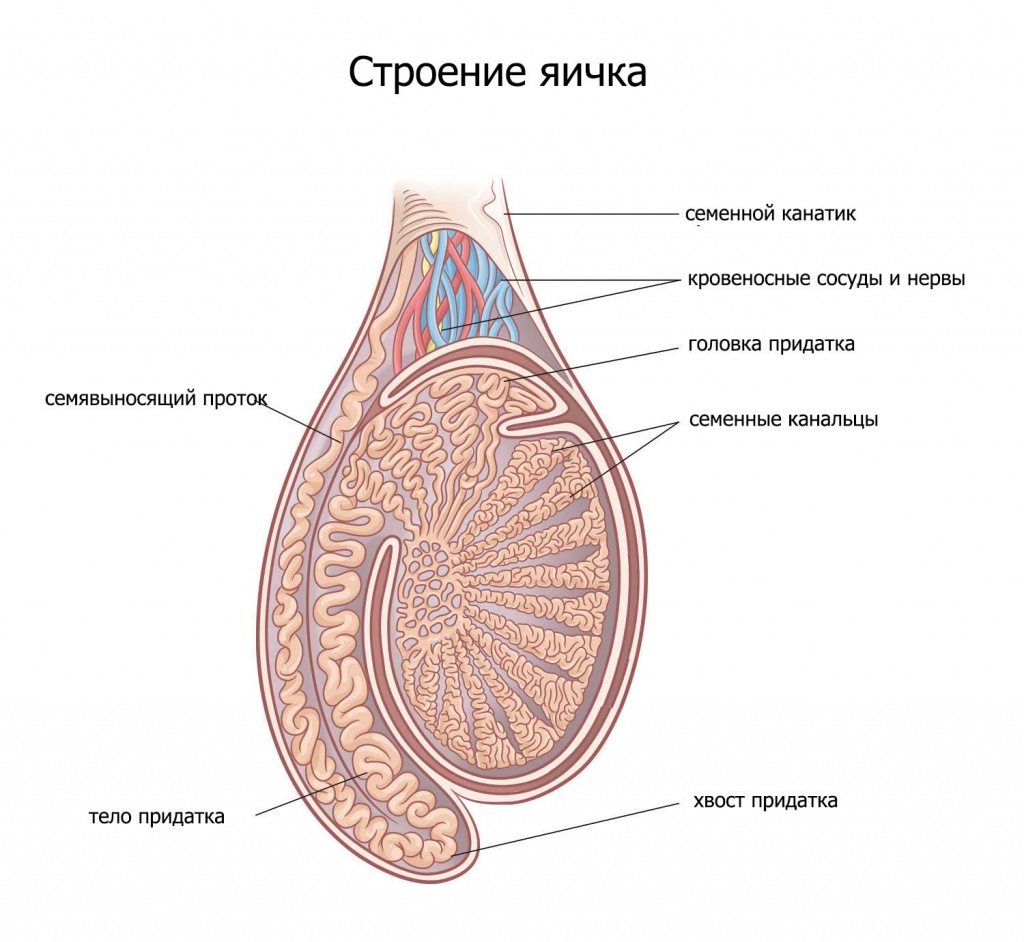
В яичках есть целая система крошечных трубок — извитых семенных канальцев. Эти трубки заполнены зародышевыми круглыми клетками, которые под действием тестостерона начинают делиться и превращаться в сперматозоиды прямо внутри стенки такой трубки. Всё это время их питают и защищают клетки Сертоли. Как только у сперматозоида формируется голова и хвост (жгутик), он проходит сквозь клетки Сертоли (гемато-тестикулярный барьер) и попадает в просвет трубки (канальца) и уже по нему начинает движение к придатку (эпидидимис).
В придатках ( а их у мужчины 2 — по одному у каждого яичка) сперматозоиды накапливаются и хранятся в течении почти 5 недель.
Параллельно с этим, предстательная железа и семенные пузырьки производят семенную плазму — беловатую жидкость, с которой смешиваются сперматозоиды и плавают в ней, попадая в семявыносящие протоки непосредственно перед эякуляцией.
Мужчина возбуждается, стимулирует половой член (мастурбация или половой акт), мышцы члена сжимаются и проталкивают эту смесь в уретру. Так мужчина эякулирует спермой — т.е. смесью семенной плазмы и сперматозоидов. В каждой порции спермы может быть до 500 миллионов сперматозоидов.
Сперматогенез и оогенез
Процесс развития мужских половых клеток (сперматогенез) и женских половых клеток (оогенез) проходит ряд периодов (рис. 222). В сперматогенезе различают четыре периода: размножение, рост, созревание и формирование.
Рис. 222. Схема сперматогенеза, оогенеза и оплодотворения
Сперматогенез проходит в семенных извитых канальцах яичек, в стенке которых имеются сперматогонии (клетки полового зачатка), размножающиеся на протяжении почти всей жизни (период размножения). Часть сперматогониев, начиная с периода полового созревания, прекращает размножение и вступает в период роста, превращаясь в сперматоциты, I порядка. Эти клетки увеличиваются в размерах, и в них происходит сложная перестройка ядерного (хромосомного) вещества. В период созревания сперматоцит I порядка делится на два сперматоцита II порядка, а из последних путем нового деления образуются четыре небольших по размерам сперматиды. При этом в сперматидах оказывается одинарное число хромосом в отличие от сперматоцитов, в которых находится двойное число хромосом. В большинстве тканевых клеток человека имеются двойной набор хромосом. Мужские и женские половые клетки содержат одинарный набор хромосом. При оплодотворении происходит слияние хромосом мужской и женской половых клеток, т. е. в зиготе образуется двойной набор хромосом (см. рис. 222).
В период формирования сперматиды приобретают черты строения сперматозоидов. Появляются головка с чехликом, а также жгутик.
Оогенез проходит периоды размножения, роста и созревания. Период формирования отсутствует. Период размножения, т. е. размножение клеток полового зачатка (оогониев), заканчивается в яичниках к моменту рождения ребенка. К этому времени в яичниках имеется определенное число ооцитов I порядка (незрелых половых клеток). Начиная с периода полового созревания один раз в 4 недели, как правило, один ооцит I порядка вступает в период роста: увеличиваются в размерах его ядро и цитоплазма; в цитоплазме происходит накапливание белков, жиров и жироподобных веществ (желтка). В это же время происходит сложная перестройка ядерного вещества. Период роста сменяется периодом созревания, сущность которого сводится к делению ооцита I порядка на ооцит II порядка (крупная клетка) и очень маленькое по размерам первое редукционное тельце. Период созревания заканчивается отделением от ооцита II порядка второго редукционного тельца, тоже маленького по размерам, и появлением в результате этого зрелой женской половой клетки (яйцеклетки).
В процессе выделения первого и второго редукционных телец яйцеклетка получает одинарный набор хромосом (как и сперматиды при сперматогенезе).
Стадии сперматогенеза
В процессе сперматогенеза выделяют четыре фазы:
- Деление.
- Рост.
- Созревание.
- Формирование.
Стадия деления
В самом крайнем ряду, у базальной мембраны, располагаются сперматогонии — мелкие округлые клетки. По сути, это стволовые клетки для будущих гамет. Часть их активно делится, «сдвигая» дочерние клетки к центру извитого канальца. На этом этапе будущие половые клетки содержат полный набор хромосом — 23 пары. Некоторые (те, что остаются у базальной мембраны) продолжают активно делиться, остальные начинают дифференцировку (формирование), превращаясь в сперматоциты первого порядка, все еще имеющие 46 хромосом.
Стадия роста
Сперматоциты первого порядка крупнее своих «прародителей», и в них идет активный обмен веществ, необходимый для подготовки к делению. Синтезируются белки, ферменты, удваивается ДНК.
Стадия созревания
На этой стадии сперматоциты первого порядка делятся дважды. После первого деления образуются сперматоциты второго порядка, имеющие 23 пары хромосом, которые сразу же делятся снова, и на этот раз каждой дочерней клетке — сперматиде — достается только одна хромосома из пары. Такое двойное деление, после которого клетка сохраняет только половинный набор хромосом, называется мейоз. В итоге из одного сперматоцита первого порядка получается 4 сперматиды. Половина из них содержит Х-хромосому, формирующую плод женского пола, половина — У-хромосому, необходимую для мужского генотипа.
Формирующиеся половые клетки по-прежнему крепко связаны с клетками Сертоли, обеспечивающими их питанием. Более того, они продолжают быть связанными и между собой мостиками из цитоплазмы. Это позволяет полноценно созреть и сформироваться клеткам, содержащим всего 23 хромосомы — количество, недостаточное для нормального существования клетки.
Стадия формирования
Формирование сперматозоидов из сперматид происходит в центральных рядах сперматогенного эпителия. Клетки отращивают жгутики, которые «свешиваются» в просвет канальцев. В жгутики смещается большая часть митохондрий — «энергетических станций» клетки. Именно они будут обеспечивать энергией движения «хвостика», обеспечивающие, собственно, возможность поступательного перемещения сперматозоидов, без которого сперма теряет фертильность.
А вот аппарат, обеспечивающий концентрацию ферментов — комплекс Гольджи — наоборот, перемещается к переднему концу головки, уплотняется и создает акросому. В ней содержатся ферменты, которые «растворяют» участок оболочки яйцеклетки, чтобы произошло оплодотворение. Сперматозоиды без акросомы не фертильны.
Только после созревания сперматозоидов разрывается цитоплазматический мостик, соединявший клетки, и полноценная гамета становится полностью автономной.
Зрелые сперматозоиды продвигаются в семявыносящие пути, соединяется с секретом предстательной железы, который обеспечивает подвижность и жизнеспособность сперматозоидов, и покидают организм во время эякуляции.
Смотрите по теме: Сколько живут сперматозоиды в разных средах
Бластоциста
Когда морула попадает в полость матки, через прозрачную зону с микроокружения эмбриона начинает просачиваться жидкость, которая накапливается в межклеточных пространствах внутренней клеточной массы. Постепенно межклеточные пространства сливаются и формируют единую полость — бластоцель. Клетки внутренней клеточной массы образуют эмбриобласт и локализованы на одном полюсе, тогда как клетки наружной клеточной массы или трофобласт, становятся плоскими и образуют стенку бластоцисты. Прозрачная зона исчезает, что дает возможность бластоцистам осуществить имплантацию.
Клетки трофобласта, которые локализуются над эмбриобластным полюсом бластоцисты, около шестого дня начинают врастать в эпителий эндометрия — слизистой оболочки матки. Прикрепление и инвазия трофобласта обеспечиваются действием интегринов, выделяемых клетками трофобласта, а также ламинином и фибронектином межклеточного матрикса эндометрия.
Имплантация является результатом комплексных взаимодействий трофобласта и эндометрия. К концу первой недели развития зародыш человека проходит стадию морулы, бластоцисты и начинает имплантацию в слизистую оболочку матки. Итак, имплантация происходит в конце первой недели развития.
Клинические корреляции. Аномальные зародыши обычно погибают через 2-3 нед после оплодотворения, поэтому их частоту определить трудно. Полагают, что около 50% беременностей заканчиваются самопроизвольными выкидышами, и половина из них обусловлена хромосомными аномалиями. Эти выкидыши является следствием так называемых «пренатальных фильтров», что отбраковывают аномальные эмбрионы и тем самым уменьшают количество индивидов с врожденными пороками до 2-3% вместо 12%.
При комбинации методов экстракорпорального оплодотворения и полимеразной цепной реакции (ПЦР) проводится молекулярный скрининг эмбрионов с генетическими аномалиями (преимплантационная диагностика). Для этого достаточно выделить один бластомер из эмбриона ранней стадии развития и реплификовать его ДНК для дальнейшего исследования. Программа «Геном человека» занимается изучением связи специфических генов с различными клиническими синдромами.
Также в разделе
| Пренатальный скрининг; хромосомные аномалии Частота врожденных пороков развития составляет 2-3%, еще 5% новорожденных имеют так называемые малые аномалии. Причинные факторы их являются гетерогенными и… | |
| Синдром частичной трисомии по короткому плечу хромосомы 9 (9р+) Синдром частичной трисомии по короткому плечу хромосомы 9 (9р+) — наиболее частая форма частичных трисомии (опубликовано около 200 сообщений о больных с такой… | |
| Синдром Хатчинсона-Гилфорда (прогерия детей) Синдром Хатчинсона-Гилфорда , или прогерия детей , — крайне редкое заболевание. Его частота составляет 1 на 1 000 000 человек. Именно этот синдром занесен под… | |
| Прогерия (преждевременное старение) Прогерия (греч. progērōs преждевременно состарившийся) — патологическое состояние, характеризующееся комплексом изменений кожи, внутренних органов,… | |
| Синдром Эдвардса (трисомия 18) Почти во всех случаях синдром Эдвардса обусловлен простой трисомнои формой (гаметическая мутация у одного из родителей). Встречаются и мозаичные формы… | |
| Клиническая диагностика наследственных болезней Большинство наследственных болезней имеет хроническое течение, вследствие чего повторная обращаемость при таких болезнях высокая. Особенно много больных с… | |
| Синдрома Вернера (прогерия взрослых) Синдрома Вернера ( прогерия взрослых) — редкое наследственное аутосомно-рецессивное соединительнотканное заболевание (М1М 272 700). Проявляется преждевременным… | |
| Синдромы частичных анеуплоидий Помимо полных трисомий и моносомий известны синдромы, связанные с частичными трисомиями и моносомиями практически по любой хромосоме. Однако эти синдромы… | |
| Синдром Марфана Синдром Марфана — наследственная доминантная болезнь соединительной ткани. Клиническая идентификация синдрома была сделана В. Марфаном в 1886 г. Причиной… | |
| Синдром Вольфа-Хиршхорна (частичная моносомия 4р-) Синдром Вольфа-Хиршхорна (частичная моносомия 4р-) — синдром, обусловленный делецией сегмента короткого плеча хромосомы 4. Клинически синдром Вольфа-Хиршхорна… |
Этапы
Весь процесс сперматогенеза можно разбить на несколько отдельных этапов, каждая из которых соответствует определенному типу клеток человека. В следующей таблице плоидность, число копий и количество хромосом / хроматид приведены для одной клетки, как правило, до синтеза и деления ДНК (в G1, если применимо). Первичный сперматоцит задерживается после синтеза ДНК и перед делением.
| Тип ячейки | плоидность / хромосомы у человека | Число копий ДНК / хроматиды у человека | Процесс введен ячейкой |
| сперматогоний (типы Ad, Ap и B) | диплоид (2N) / 46 | 2C / 46 | сперматоцитогенез ( митоз ) |
| первичный сперматоцит | диплоид (2N) / 46 | 4C / 2×46 | сперматидогенез (мейоз I) |
| два вторичных сперматоцита | гаплоид (N) / 23 | 2C / 2×23 | сперматидогенез (мейоз II) |
| четыре сперматиды | гаплоид (N) / 23 | С / 23 | спермиогенез |
| четыре функциональных сперматозоида | гаплоид (N) / 23 | С / 23 | семяизвержение |
Сперматоцитогенез
Процесс сперматогенеза, когда клетки переходят от первичных сперматоцитов ко вторичным сперматоцитам, сперматидам и сперматозоидам.
Цикл семенного эпителия яичка
Сперматоцитогенез является мужской формой гаметоцитогенеза и приводит к образованию сперматоцитов, обладающих половиной нормального набора генетического материала. В сперматоцитогенезе диплоидный сперматогоний , который находится в базальном отделе семенных канальцев, митотически делится, производя две диплоидные промежуточные клетки, называемые первичными сперматоцитами . Затем каждый первичный сперматоцит перемещается в адлюминальный отсек семенных канальцев и дублирует свою ДНК, а затем подвергается мейозу I с образованием двух гаплоидных вторичных сперматоцитов , которые позже снова делятся на гаплоидные сперматиды . Это деление подразумевает источники генетической изменчивости, такие как случайное включение одной из родительских хромосом и кроссовер хромосом, который увеличивает генетическую изменчивость гамет. Механизм реакции на повреждение ДНК (DDR) играет важную роль в сперматогенезе. Белок FMRP связывается с мейотическими хромосомами и регулирует динамику аппарата DDR во время сперматогенеза. FMRP, по-видимому, необходим для восстановления повреждений ДНК .
Каждое деление клетки от сперматогония до сперматиды неполное; клетки остаются связанными друг с другом мостиками цитоплазмы, что обеспечивает синхронное развитие. Не все сперматогонии делятся с образованием сперматоцитов; в противном случае запасы сперматогоний закончились бы. Вместо этого сперматогониальные стволовые клетки делятся митотически, чтобы производить копии самих себя, обеспечивая постоянный приток сперматогониев для подпитки сперматогенеза.
Сперматидогенез
Сперматидогенез — это создание сперматид из вторичных сперматоцитов. Вторичные сперматоциты, полученные ранее, быстро входят в мейоз II и делятся с образованием гаплоидных сперматид. Краткость этого этапа означает, что вторичные сперматоциты редко выявляются при гистологических исследованиях.
Спермиогенез
Во время спермиогенеза сперматиды начинают формировать хвост за счет роста микротрубочек на одной из центриолей, которая превращается в базальное тело. Эти микротрубочки образуют аксонему . Позже центриоль модифицируется в процессе . Передняя часть хвоста (называемая средней частью) утолщается, потому что митохондрии расположены вокруг аксонемы, чтобы обеспечить снабжение энергией. ДНК сперматид также подвергается упаковке, становясь сильно конденсированной. ДНК сначала упаковывается со специфическими основными белками ядра, которые впоследствии заменяются протаминами во время удлинения сперматид. Получающийся в результате плотно упакованный хроматин транскрипционно неактивен. Аппарат Гольджи окружает теперь конденсированное ядро, становясь акросомой .
Созревание происходит под действием тестостерона, который удаляет оставшуюся ненужную цитоплазму и органеллы . Избыточная цитоплазма, известная как остаточные тельца , фагоцитируется окружающими клетками Сертоли в семенниках . Полученные сперматозоиды теперь созрели, но не имеют подвижности. Зрелые сперматозоиды высвобождаются из защитных клеток Сертоли в просвет семенных канальцев в процессе, называемом спермией .
Неподвижные сперматозоиды переносятся к придатку яичка в тестикулярной жидкости, секретируемой клетками Сертоли с помощью перистальтического сокращения . Находясь в придатке яичка, сперматозоиды приобретают подвижность и становятся способными к оплодотворению. Однако транспортировка зрелых сперматозоидов через оставшуюся часть мужской репродуктивной системы достигается за счет сокращения мышц, а не недавно приобретенной подвижности сперматозоидов.
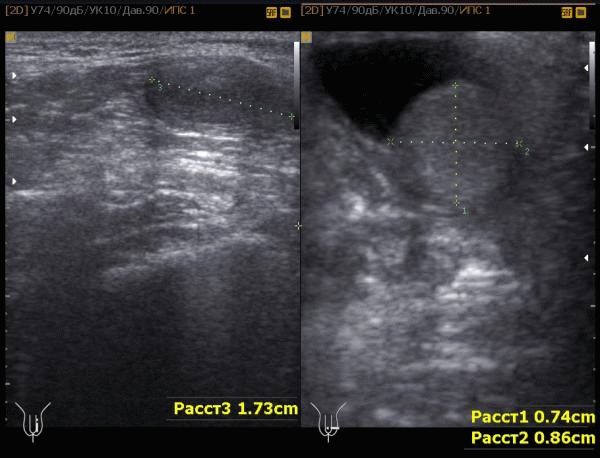
Варикоцеле и бесплодие
Варикоцеле — расширение вен яичка вследствие рефлюкса крови по системе яичковой вены. Варикоцеле наблюдается в 15% общей популяции мужчин. Сочетание варикоцеле и первичного бесплодия наблюдается в 35%, вторичного бесплодия и варикоцеле в 80%. В ряде случаев для определения венозного рефлюкса требуется проведение дополнительного ультрасонографического исследования. Необходимо помнить, что между степенью выраженности варикоцеле и качеством эякулята прямая корреляция отсутствует.
При сочетании варикоцеле и любой других клинических и лабораторных изменений за исключением обструктивной симптоматики и эякуляторной дисфункции первым этапом целесообразно провести лечение варикоцеле.
Для лечения варикоцеле предложено несколько оперативных методов. Необходимо различать обструктивные и необструктивные методики хирургического лечения варикоцеле. К первым относятся операция Иваниссевича, Мармара, Паломо, лапароскопическая варикоцелэктомия, трансфеморальная эмболизиция яичковой вены, а также микрохирургическое лигирование вен семенного канатика из минидоступа.
К необструктивное методике относится формирование микрохирургических венозных анастомозов — тестикуло-нижнеэпигастрального и тестикуло-сафенного. Метод тестикулярно-эпигастрального анастомозирования позволяет дренировать кровь из гроздьевидного сплетения в систему подвздошной вены при I, а также при II и III типах, если причина рефлюкса не связана с клапанной недостаточностью вен из системы сброса в левую подвздошную вену.
В настоящее время показания к хирургическому лечению варикоцеле пересматриваются. Поскольку между степенью выраженности варикоцеле и степенью снижения фертильности прямая зависимость отсутствует, считаем показаниями к оперативному лечению варикоцеле стойкое снижение фертильности эякулята, болевую симптоматику и выраженный эстетический дефект в области мошонки.
В настоящее время в литературе появляется все больше сообщений о том, что у пациентов с варикоцеле и нормалыми показателями спермограммы после операции наблюдается появление антиспермальных антител и ухудшение параметров эякулята, что, по всей видимости, может быть связано с ухудшением трофики яичка после проведения обструктивной операции. В свете этого мы полагаем, что операция с использованием микрососудистого метода в целях формирования венозного анастомоза и нормализации оттока крови из системы яичковой вены представляется более предпочтительной по сравнению с традиционными обструктивными методиками.
Варикоцеле — не приговор! Методы лечения варикоцеле (информация для врачей) Микрохирургическое лечение варикоцеле. Тестикуло-нижнеэпигастральный анастомоз Клинический пример — Микрохирургическое лечение варикоцеле
Роль клеток Сертоли
Обозначенная диаграмма организации клеток Сертоли (красный цвет) и сперматоцитов (синий цвет) в семеннике. Сперматиды, которые еще не прошли спермиевание, прикрепляются к верхушке просвета клетки.
На всех стадиях дифференцировки сперматогенные клетки находятся в тесном контакте с клетками Сертоли, которые, как считается, обеспечивают структурную и метаболическую поддержку развивающихся сперматозоидов. Одиночная клетка Сертоли простирается от базальной мембраны до просвета семенного канальца, хотя цитоплазматические отростки трудно различить на уровне световой микроскопии.
Клетки Сертоли выполняют ряд функций во время сперматогенеза, они поддерживают развивающиеся гаметы следующим образом:
- Поддерживать среду, необходимую для развития и созревания, через гемато-яичковый барьер
- Секретные вещества, инициирующие мейоз
- Секрет поддерживающей тестикулярной жидкости
- Выделяет андроген-связывающий белок (ABP), который концентрирует тестостерон
Тестостерон необходим в очень больших количествах для поддержания репродуктивного тракта, а АД обеспечивает гораздо более высокий уровень фертильности.
в непосредственной близости от развивающихся гамет.
- Секретные гормоны, влияющие на контроль гипофиза над сперматогенезом, особенно полипептидный гормон ингибин
- Остаточная цитоплазма фагоцитоза, оставшаяся после спермиогенеза
- Секреция антимюллерова гормона вызывает ухудшение мюллерова протока.
- Защищают сперматиды от иммунной системы мужчины через барьер кровь-яички
- Вклад в нишу сперматогониальных стволовых клеток
В межклеточной адгезии ICAM-1 и растворимым ICAM-1 , имеют антагонистические эффекты на плотных соединений , образующих гематоэнцефалический барьер семенников. Молекулы ICAM-2 регулируют адгезию сперматид на апикальной стороне барьера (по направлению к просвету ).
Характеристики овогенеза и сперматогенеза
Половые клетки в сперматогенезе носят название сперматозоидов, а в овогенезе яйцеклетками. Как известно, чтобы произошел процесс оплодотворения, нужно чтобы мужская гамета попала в женскую.
В сравнении овогенеза и сперматогенеза нельзя не отметить различные размеры гамет мужских и женских особей. Яйцеклетка намного больше сперматозоидов, поскольку она в течение всего периода вбирает в себя множество полезных и питательных веществ. При этом после созревания мужские гаметы становятся подвижными, благодаря чему могут легко преодолевать половые пути женщин. Женские же гаметы остаются неподвижными в все время, в ходе которого происходит подготовка яйцеклетки к оплодотворению.
Если рассматривать овогенез и сперматогенез в таблице, можно будет заметить, что этапы, на которых происходит увеличение в размерах, деление и полное созревание у обоих полов, совпадают. Схемы овогенеза и сперматогенеза очень схожи, однако развитие сперматозоидов включает в себя еще и четвертую стадию, которая заключается в окончательном оформлении.
Еще одной особенностью сперматогенеза и овогенеза являются различные периоды выработки мужских и женских половых клеток. Яйцеклетки образуются в организме женщины циклически, с чем и связан менструальный цикл. Образование новой яйцеклетки происходит каждые 21-35 дней. В конце цикла яйцеклетка погибает, данный процесс сопровождается кровотечением. Вследствие этого происходят изменения в гормональном фоне, в результате которых запускается новый процесс созревания яйцеклетки.
У мужчин же образование сперматозоидов происходит постоянно, причем выработка гамет происходит в течение всего периода зрелости мужчины. В день у мужчины производится порядка 30 миллионов сперматозоидов. У женщины же количество гамет намного меньше. Для сравнения, за всю жизнь у представительниц прекрасного пола вырабатывается около 500 зрелых половых клеток.
Сперматогенез в отличие от овогенеза более подвержен воздействию внешних условий. Это связано в первую очередь с тем, что половые железы, или семенники у мужчин находятся вне брюшной полости, то есть в яичках.
Стадия роста в овогенезе значительно превышает аналогичную стадию в сперматогенезе, чем и объясняется, что яйцеклетка намного больше по размерам, чем сперматозоиды. Зато мужские гаметы компенсируют этот этап делением клеток и образованием большого количества спермиев.
Эти особенности сперматогенеза и овогенеза имеют биологический смысл, который связан с разным назначением мужских и женских гамет. Неравномерное деление клеток при овогенезе (меньше) обеспечивает формирование крупной яйцеклетки, в ней накапливается большее количество питательных веществ, так как из оплодотворенного яйца будет развиваться новый организм.
При сравнительной характеристике овогенеза и сперматогенеза можно заметить, что сперматозоидов образуется значительно больше, и это также имеет биологический смысл.Яйцеклетку достигает только один сперматозоид, проникает в нее и доставляет свой набор хромосом. Остальные же в процессе поиска яйцеклетки массово погибают.
При сравнении овогенеза и сперматогенеза становится понятным, почему сперматозоидам нет необходимости в запасании питательных веществ – их существование кратковременно, а подвижность должна быть высокой.
Вспомогательные репродуктивные технологии (ВРТ)
Под вспомогательными репродуктивными технологиями подразумеваются:
- Внутриматочная инсеминация спермой мужа.
- Экстракорпоральное оплодотворение.
- Экстракорпоральное оплодотворение с микроманипуляцией ICSI (ИКСИ)
- Использование спермы донора во ВРТ.
Введение сперматозоидов непосредственно в полость матки предусматривает искусственное прохождение шейки матки сперматозоидами, которые могли бы погибнуть при цервикальном факторе бесплодия при попытки е стественного зачатия.
Показаниями к внутриматочной инсеминации также являются эякуляторная дисфункция, иммунологическое бесплодие, олигоастенозооспермия.
Иммунологический фактор бесплодия преодолевается путем предварительной обработки сперматозоидов. В случае неизвестной этиологии бесплодия также возможно искусственное оплодотворение методом внутриматочной инсеминации при удовлетворительных показателях качества эякулята (количество подвижных сперматозоидов более 5 млн.). Инсеминация спермы донора позволяет избежать непосредственного полового акта.
Методика экстракорпорального оплодотворения, предусматривает стимуляцию суперовуляции, что может вызвать ряд осложнений, как непосредственно при стимуляции, так вследствие многоплодной беременности. Успех процедуры стимуляции в большой степени зависит от состояния эндокринной системы женщины. Известно, что частота наступления беременности выше в тех случаях, когда при пункции фолликулов удается аспирировать более 5 яйцеклеток. Далее ооциты аспирируются путем трансвагинальной пункции яичников. После этого происходит оплодотворение in vitro — экспозиция яйцеклеток в одной среде с обработанными сперматозоидами. Затем следует перенос эмбрионов в полость матки и редукция части эмбрионов.
Возможности коррекции азооспермии оставались минимальными до внедрения методики инъекции сперматозоида в цитоплазму зрелой яйцеклетки (ICSI), требующей для оплодотворения лишь единичных сперматозоидов эпидидимального или тестикулярного происхождения.
Показаниями к ЭКО (ICSI) является: концентрация сперматозоидов ниже 10 млн. (2 млн. для ИКСИ), подвижность сперматозоидов 2 — меньше 10% (5% для ICSI), более 70% патологических форм сперматозоидов (более 96 для ИКСИ), возможность получения сперматозоидов только хирургическим путем, безуспешность других методов лечения.
Эффективность методов искусственного оплодотворения составляет около 30% за одну попытку.
Применение вспомогательных репродуктивных технологий значительно расширяет возможности коррекции наиболее тяжелых форм мужского бесплодия, включая азооспермию. Грамотное и эффективное лечение бесплодного брака возможно только при осуществлении четкого взаимодействия между урологами, гинекологами и специалистами ЭКО. Обязательным является полное информирование пациента обо всех возможных методах восстановления фертильности с указанием процента успешных мероприятий и риска развития осложнений у него самого и его супруги.
Азооспермия. Лечение бесплодия
Необходимо различать обструктивную азооспермию (экскреторное бесплодие) и необструктивную (секреторное бесплодие) азооспермию, либо выраженную патоспермию.
Для обструктивной азооспермии характерны нормальные размеры яичек, нормальный уровень гормонов, отсутствие клеток сперматогенеза в центрифугированном эякуляте, воспалительные заболевания половых органов, операции на органах мошонки и малого таза, а также пальпаторное определение патологии придатков и семявыносящих протоков.
При необструктивной азооспермии наблюдаются признаки гипогонадизма, единичные сперматозоиды или клетки сперматогенеза в эякуляте, гормональные сдвиги, генные и хромосомные изменения, в анамнезе — токсические влияния, орхит.
Оптимальным способом лечения обструктивной азооспермии является выполнение микрохирургического восстановления семявыносящих путей с одномоментным получением сперматозоидов из зоны, располагающейся проксимальнее обструкции.
Полученный материал может быть одновременно использован в цикле ЭКО-ICSI. При этом часть сперматозоидов подвергается криоконсервации и используется в случае безуспешной операции.
Более сложным вопросом является лечение в программе ЭКО-ICSI пациентов с необструктивными формами бесплодия. Оптимальным способом получения сперматозоидов при необструктивной азооспермии в цикле ЭКО-ICSI является билатеральная мультифокальная биопсия яичек с использованием микрохирургической техники.
Известно, что при необструктивной азооспермии может быть сохранен фокальный сперматогенез. В независимости от полученных результатов гормонального и генетического исследования даже при гипергонадотропном гипогонадизме при билатеральной мультифокальной микрохирургической биопсии возможно получение сперматозоидов (до 65%).
При необструктивной азооспермии на фоне гипогонадотропного гипогонадизма первым этапом следует провести стимулирующую терапию гонадотропинами.
При выраженной патоспермии на фоне генетических аномалий, гипогонадизма (кроме гипогонадотропного), обструктивной симптоматики, варикоцеле, отсутствии АСАТ — возможно проведение эмпирической терапии, при отсутствии эффекта (либо сразу) пациент включается в программу вспомагательных репродуктивных технологий.
При необструктивной азооспермии, азооспермии неясного генеза, патоспермии любой степени выраженности (за исключением доказанной односторонней обструкции) первым этапом необходимо исключить варикоцеле, в том числе субклиническое. Проведение стимулирующей терапии целесообразно после лечения варикоцеле.
При сочетании необструктивной (неясного генеза) патоспермии (азооспермии) и антиспермальных антител проведение стимулирующего лечения противопоказано.
При идиопатическом бесплодии возможно проведение лечения гонадотропинами или антиэстрогенами, а также витаминотерапия и растительными стимуляторами сперматогенеза со сбалансированным содержанием микроэлементов. Однако эффективность такого лечения бесплодия не превышает 5%.
- Реконструкция семявыносящих путей при обтурационной азооспермии
- Восстановление семявыносящего протока после ятрогенного повреждения
- Реконструкция семявыносящих путей при обтурационной аспермии
- Азооспермия — клинический пример
Установите Flash Player для просмотра видео.