Саркома
Содержание:
- Клиническая картина
- Лечение
- Лечение саркомы мягких тканей
- Лечение
- Лучевая терапия
- Симптомы опухолей слюнных желез
- Методы диагностики саркомы Юинга
- Какие бывают виды опухоли? Что мы знаем о её микроскопических (гистологических) особенностях?
- Какие шансы вылечиться от остеосаркомы?
- Список литературы
- Другие заболевания из группы Онкологические заболевания:
- Классификация и стадии
- Лечение
Клиническая картина
Саркома Юинга и примитивные нейроэктодермальные опухоли могут развиваться в любых костях, поражая и мягкие окружающие ткани. Практически половина сарком Юинга затрагивает нижние конечности и тазовую область. Часто в патологический процесс вовлекаются и кости верхних конечностей. ПНЭО чаще всего поражают кости и мягкие ткани грудной клетки, легкие, органы средостения и плевру.
Основным признаком патологии является болевой синдром. Сначала боль слабо выражена, может самопроизвольно ослабевать или даже исчезать на некоторое время. Но по мере развития онкологического процесса боль прогрессирует и становится более ощутимой. Все пациенты с костной саркомой отмечают отечность в области развития опухолевого процесса. Припухлость постепенно захватывает окружающие суставные поверхности, провоцируя нарушение подвижности сустава и конечности в целом.
Во время пальпации зона отека болезненная, отличается выраженной гиперемией, увеличением сосудистого рисунка и пастозностью, горячая на ощупь. Наблюдается умеренное увеличение лимфатических узлов. Если опухоль развивается в области таза, то могут возникать нарушения функционирования внутренних органов этой зоны (недержание кала, мочи, параличи). Боль склонна усиливаться в ночное время суток, часто она не поддается купированию традиционными методами. При увеличении опухолевых клеток повышается нагрузка на кости, вследствие чего могут возникать переломы.
Часть пациентов на момент выявления болезни отмечает признаки интоксикации: больные жалуются на слабость, снижение массы тела, незначительное повышение температуры тела. Опухоли этого семейства склонны очень быстро давать метастазы в легкие, костный мозг, кости.
Многие пациенты не обращаются за медицинской помощью при появлении боли и отечности, так как относят эти симптомы к незначительному воспалению, развивающемуся после травмы или перенесенного заболевания. Из-за поздней диагностики опухоли до принятия эффективных лечебных мероприятий уже развивается выраженное метастазирование, в результате которого лечение саркомы Юинга и ПНЭО часто бывает малоэффективным
Крайне важно своевременно обращаться к докторам, как только возникают ранние признаки патологии
Саркомы необходимо лечить только в специализированных клиниках, обладающим современным диагностическим оборудованием и опытом ведения пациентов с подобными заболеваниями. Современная медицина, увы, несовершенна, многие доктора некомпетентны, а промедление в данном случае просто недопустимо. Пациенты с саркомами нуждаются в лечении у настоящих профессионалов.
Самое важное — диагностика и своевременное лечение. Настаивайте на прохождении обследования, даже если доктор не видит в этом необходимости
Пациент — активный участник лечебного процесса. Многие специалисты уже давно признали этот факт и с успехом внедряют его в свою современную практику.
Лечение
Лечение саркомы мягких тканей
Выбор метода лечения саркомы определяется степенью ее злокачественности, местом расположения и наличием метастазов. Для лечения низкозлокачественных опухолей, лечение преимущественно хирургическое, в остальных случаях используются комбинированные методы, включающие облучение и химиотерапию.
Хирургическое лечение
При хирургическом лечении сарком используются следующие виды операций:
- Широкая местная резекция. Таким способом удаляются низкозлокачественные небольшие новообразования, располагающиеся в коже и подкожной клетчатке.
- Широкое иссечение. При таком вмешательстве саркома удаляется в пределах анатомической зоны, отступая от края новообразования не менее чем на 4-6 см.
- Радикальная органосохраняющая операция. При таком объеме вмешательства удаляется опухоль совместно с мышечными фасциями и неизмененными мышцами, которые отсекаются в месте их прикрепления. При вовлечении в процесс кровеносных сосудов, нервных стволов и костей, производят их резекцию с одномоментной пластикой кожным или кожно-мышечным лоскутом.
- Ампутации или экзартикуляции — удаление конечности или ее вычленение по линии суставной щели. Такие вмешательства проводятся при обширных местно-распространенных высокозлокачественных процессах с вовлечением магистральных кровеносных и нервных стволов на большом протяжении, а также костных структур и мышц.
Во время операции обязательно проводится интраоперационное срочное гистологическое исследование. При наличии злокачественных клеток в краях отсечения и при потенциальной возможности радикального удаления опухоли, выполняют реоперацию.
Лучевая терапия
Лучевая терапия применяется в рамках комбинированного лечения в предоперационном и/или послеоперационном этапе. В первом случае преследуется цель — уменьшение размера саркомы и создание условий для проведения радикального вмешательства. Во втором — уничтожение оставшихся злокачественных клеток. Чтобы воздействие на опухоль было равномерным, используются многопольные методики облучения.
Предоперационная лучевая терапия
При предоперационной ЛТ, границы полей облучения (ПО) должны выходить за размеры ткани опухоли минимум на 3-4 см. Если опухоль имеет большие размеры, производят облучение в пределах 10 см от ее края до достижения суммарной очаговой дозы 45-50Гр. Затем ПО сокращают до размеров новообразования.
Если опухоль располагается на конечности, есть вероятность развития остеолучевого некроза, мышечных контрактур и отеков. Чтобы этого избежать, рекомендуется облучать не более 2/3 окружности конечности, если это возможно. Минимальная толщина необлучаемых тканей в зоне предплечья составляет 2 см, на бедре 4 см, и на голени — 3 см.
Послеоперационная лучевая терапия
Послеоперационная лучевая терапия показана в следующих случаях:
- Высокая степень злокачественности саркомы по данным гистологического исследования.
- Нерадикально проведенная операция — наличие злокачественных клеток в краях отсечения при невозможности проведения реоперации.
- Вскрытие капсулы саркомы во время хирургического вмешательства.
Послеоперационную ЛТ начинают выполнять не позднее, чем через 4 недели после окончания хирургического лечения.
Если предоперацинная ЛТ не выполнялась, поля облучения включают в себя следующие области:
- Ложе опухоли.
- Ткани, которые располагаются на расстоянии 2 см от удаленной опухоли.
- Послеоперационный рубец.
Облучение проводят в суммарной очаговой дозе 60 Гр. Если была проведена нерадикальная операция, дозу увеличивают до 70 Гр. В аналогичном режиме проводят лучевую терапию при невозможности оперативного лечения.
Химиотерапия
Химиотерапия широко используется для лечения высокозлокачественных сарком мягких тканей. Как и при лучевой терапии, ее могут назначать на дооперационном и/или послеоперационном этапе. Неоадъювантная (предоперационная) ХТ призвана воздействовать на очаг опухоли, уничтожать микрометастазы и создать условия для органосохраняющего хирургического лечения. С этой целью проводят 2-3 курса химиотерапии с перерывом в 3-4 недели.
Послеоперационная ХТ может проводиться для уничтожения микрометастазов или уже визуализируемых метастазов. С этой целью выполняют 3-4 курса лечения. При химиотерапевтическом лечении сарком применяют различные комбинации следующих препаратов:
- Доксорубицин.
- Этопозид.
- Винкристин.
- Ифосфамид.
- Дакарбазин.
- Цисплатин и др.
Схема химиотерапии будет определяться морфологическим вариантом опухоли и ее чувствительностью к ранее проводимому лечению.
Лечение
Лечение саркомы зависит от ее стадии и степени злокачественности. При низкой степени злокачественности и ранней степени заболевание проводится лечение у хирурга и оперативное удаление опухоли. Это позволяет восстановить функциональность органов и тканей.
При последних стадиях заболевания, а также при средней и высокой степени злокачественности хирургическое лечение комбинируют с химиотерапией и лучевой терапией. Химиотерапию и лучевую терапию проводят как до операции, так и после нее. В некоторых случаях необходимо длительное лечение. Иногда применяется виротерапия (применение в лечение онкологических вирусов).
Для данного типа заболевания характерны частые рецидивы.
Лучевая терапия
Чувствительность саркомы Юинга к облучению очень высока, поэтому лучевую терапию применяют у всех пациентов, у которых невозможно удалить опухоль, и которым противопоказано хирургическое вмешательство по состоянию здоровья. Также лучевая терапия может дополнять операцию.
Обычно облучение проводят пять дней в неделю в течение нескольких недель. Процедура напоминает рентгенографию, но во время нее применяют более высокие дозы излучения.
Современные линейные ускорители способны генерировать излучение, форма которого в точности повторяет очертания злокачественной опухоли. Это позволяет эффективно уничтожать злокачественные клетки, не причиняя вреда окружающим тканям. В современных онкологических клиниках применяются такие методики, как 3D-конформная лучевая терапия (3D-CRT), лучевая терапия с модуляцией интенсивности (IMRT).
Чтобы обеспечить высокую точность облучения, важно правильно провести подготовку к лучевой терапии. Этот процесс называется симуляцией, во время него применяют МРТ и другие методы визуализации — они помогают правильно рассчитать углы, под которыми будут направлены лучи

Симптомы опухолей слюнных желез
Доброкачественные опухоли
Из доброкачественных опухолей слюнной железы чаще всего встречается смешанная опухоль, или полиморфная аденома. В основном она располагается в околоушной железе, хотя может поразить и подъязычную, поднижнечелюстную и малые железы в щечной области. Растет опухоль очень медленно, несколько лет, и за долгий срок вполне может достигнуть значительных размеров, став причиной асимметрии лица. Боли при полиморфной аденоме не бывает, парез лицевого нерва отсутствует. В 6% случаев есть вероятность малингизации аденомы, а после удаления она иногда рецидивирует.
Еще одна доброкачественная опухоль – это мономорфная аденома, чаще всего локализующаяся не в самих слюнных железах, а в их выводных протоках. Клинически она протекает как полиморфная аденома.
Из эпителиальных опухолей еще встречаются аденолимфомы, поражающие обычно околоушную слюнную железу и непременно сопровождающиеся реактивным воспалением.
Иногда в слюнных железах развиваются не эпителиальные, а соединительнотканные опухоли, однако это случается намного реже. В детстве это в основном ангиомы: гемангиомы и лимфангиомы. В любом возрасте встречаются липомы и невриномы. Неврогенные опухоли обычно развиваются в околоушных слюнных железах, так как они исходят из ветвей лицевых нервов.
Если опухоль принадлежит к глоточному отростку околоушной железы, то возможен тризм, оталгия и дисфагия.
Промежуточные опухоли
Ацинозноклеточные, мукоэпителиальные (мукоэпидермоидные) опухоли и цилиндромы характеризуются местно-деструирующим инфильтративным ростом, так что их относят к промежуточным новообразованиям. Из них цилиндромы обычно поражают малые слюнные железы, а остальные – околоушные слюнные железы.
Обычно промежуточные опухоли развиваются не слишком быстро, однако при определенных обстоятельствах приобретают все черты злокачественных опухолей, в том числе ускоренный рост, склонность к частым рецидивам и метастазирование в кости и легкие.
Злокачественные опухоли
Такие опухоли могут возникать первично, а могут развиваться их промежуточных и доброкачественных опухолей слюнных желез.
Злокачественные опухоли слюнных желез представлены саркомами и карциномами. Для них характерно очень быстрое увеличение в размерах и инфильтрация в расположенные рядом мягкие ткани (мышцы, слизистую и кожу). Иногда кожа над пораженной железой изъязвляется или краснеет. Для злокачественных опухолей характерен парез лицевого нерва, боли, отдаленные метастазы, увеличенные регионарные лимфоузлы и контрактура жевательных мышц.
Методы диагностики саркомы Юинга
Обязательное обследование при подозрении на саркому Юинга включает:
- Рентгенографию костей, пораженных первичной опухолью и метастазами.
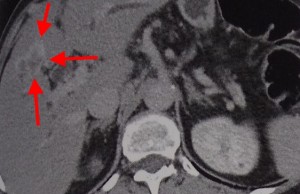
- Рентгенографию и компьютерную томографию грудной полости.
- Компьютерную томографию или МРТ всех костей и мягких тканей, пораженных опухолевым процессом.
- Позитронно-эмиссионную томографию (ПЭТ-КТ). Во время этого исследования в организм пациента вводят безопасный радиофармпрепарат, который накапливается в опухолевых очагах и делает их хорошо заметными на снимках, выполненных с помощью специального оборудования.
- Остеосцинтиграфия — исследование обмена веществ в костной ткани с помощью введенных в организм радиофармпрепаратов, которые накапливаются в костях.
Диагноз обязательно подтверждают с помощью биопсии: врач должен получить образец опухолевой ткани и отправить в лабораторию для исследования.
Зачастую прибегают к трепанобиопсии. Эту малотравматичную процедуру проводят под местной анестезией, во время нее в кость вводят специальный инструмент — трепан — в виде трубки с острым краем, напоминающей толстую иглу (отсюда второе название процедуры — толстоигольная биопсия) и, таким образом, получают столбик ткани. Толстоигольную биопсию можно провести под навигацией УЗИ и КТ, это повышает точность забора материала. Но в 20% случаев ткани для исследования может не хватить, и процедуру приходится повторять. Тут играют роль размеры, локализация опухоли, уровень мастерства врача.
Наиболее точную патоморфологическую верификацию диагноза обеспечивает открытая инцизионная биопсия. Ее применяют при сложной локализации опухоли, и если оказалась неэффективна трепанобиопсия. Во время этой процедуры делают разрез и удаляют часто саркомы. Такую операцию должен выполнять опытный хирург-ортопед. Вмешательство должно быть минимально травматичным для пациента, так как значительное повреждение кости грозит патологическим переломом.
Полученный материал исследуют в лаборатории. Проводят гистологическое исследование. Уточнить тип опухоли помогает иммуногистохимия (выявление определенных белков в опухолевой ткани), молекулярно-генетические анализы.
Какие бывают виды опухоли? Что мы знаем о её микроскопических (гистологических) особенностях?
Саркомы Юинга относятся к примитивным злокачественным опухолям. До сих пор точно не известно, какая именно клетка начинает мутировать и в результате начинает вырастать эта опухоль. Современные исследования говорят о том, что клетки саркомы Юинга вырастают из незрелых (или на языке специалистов недифференцированных) клеток ткани, это так называемые мезенхимальные .
Понять, заболел ли ребёнок саркомой Юинга, или другой злокачественной опухолью, которая тоже состоит из недифференцированных опухолевых клеток (например, это могут быть , , , и ), можно только проведя гистологический анализ и специальные молекулярно-генетические исследования. Так как все эти виды рака встречаются достаточно редко, то такую диагностику, как правило, способны выполнить только специализированные лаборатории.
В зависимости от микроскопических (гистологических) особенностей опухолевой ткани, а также от того, в каком именно месте выросла опухоль, в семействе сарком Юинга выделяют следующие типы:
- классическая сарокма Юинга (в западной литературе принято сокращение EWS)
- периферическая примитивная нейроэктодермальная опухоль (на русском языке может называться ППНЭО, в зарубежных источниках принято сокращение PPNET или pPNET)
- опухоль Аскина (опухоли грудной стенки)
- внекостная саркома Юинга
Какие шансы вылечиться от остеосаркомы?
У детей и подростков с остеосаркомой болезни зависит от нескольких причин. Главными из них являются: конкретный тип опухоли, где именно она выросла, насколько болезнь успела распространиться по организму к моменту постановки диагноза, как опухоль ответила на курс химиотерапии до операции, насколько возможным было полное хирургическое удаление опухоли.
За последние три десятилетия результаты лечения злокачественной остеосаркомы достигли большого прогресса, когда всех заболевших детей стали лечить по единым протоколам (исследования оптимизации терапии). Благодаря тому, что лечение стало комбинированным, особенно после введения интенсивных стандартизированных курсов полихимиотерапии, доля выздоравливающих составляет 60% — 70%. О благоприятном прогнозе обычно говорят, если опухоль была полностью удалена хирургическим путём и болезнь хорошо отвечала на курс химиотерапии.
Хорошие шансы на выздоровление у детей с опухолями рук или ног, которые не дали метастазы – около 70%
Но здесь очень важно, как болезнь отвечает на курс химиотерапии. Если хорошо (то есть у ребёнка после проведённого курса осталось меньше 10% живых опухолевых клеток), то это считается гораздо лучшим прогнозом по сравнению с тем, когда болезнь плохо отвечает на лечение
При плохом ответе сразу повышается риск рецидива. Шансы на то, что рецидива будет, составляют менее 50%.
Если у ребёнка опухоль выросла на туловище, или опухоль очень большого размера, то прогноз считается менее благоприятным, чем у детей с опухолями конечностей, или с небольшими опухолями
Если есть метастазы, то важно, где именно они находятся и можно ли их удалить. У детей с единичными метастазами в лёгких, которые можно хирургически удалить, шансы на выздоровление выше, чем у детей с метастазами в кости, или с многоочаговой остеосаркомой
Необходимое замечание: когда мы называем проценты выздоровевших детей, это значит, что мы даём только точную статистику по этой форме рака у детей. Но никакая статистика не может предсказать, выздоровеет конкретный ребёнок, или нет. Сам термин «выздоровление» надо понимать прежде всего как «отсутствие опухоли». Потому что современные методы лечения могут обеспечивать долговременное отсутствие злокачественной опухоли. Но у них есть нежелательные побочные эффекты и поздние осложнения. Поэтому детям после лечения нужна . Также им нужна ещё долгое время ортопедическая помощь.
Список литературы
-
Kaatsch P, Spix C: Jahresbericht 2011. Deutsches Kinderkrebsregister, Universitätsmedizin der Johannes Gutenberg-Universität Mainz 2011 [URI: http://www.kinderkrebsregister.de/ dkkr/ veroeffentlichungen/ jahresbericht/ jahresbericht-2011.html]
-
Bielack S: Osteosarkome. Leitlinie der Gesellschaft für Pädiatrische Onkologie und Hämatologie AWMF online, 2010 [URI: http://www.awmf.org/ uploads/ tx_szleitlinien/ 025-005l_S1_Osteosarkome_2011-abgelaufen.pdf]
-
Bielack S, Carrle D: Diagnostik und multimodales Therapiekonzept des Osteosarkoms. ärztliches journal reise & medizin onkologie, Otto Hoffmanns Verlag GmbH 3/2007, S: 34
-
Zoubek A, Windhager R, Bielack S: Osteosarkome. in: Gadner H, Gaedicke G, Niemeyer CH, Ritter J (Hrsg.): Pädiatrische Hämatologie und Onkologie Springer-Verlag 2006, 882
-
Bielack S, Machatschek J, Flege S, Jürgens H: Delaying surgery with chemotherapy for osteosarcoma of the extremities. Expert Opin Pharmacother 2004, 5: 1243
-
Graf N: Osteosarkome. in: Gutjahr P (Hrsg.): Krebs bei Kindern und Jugendlichen Deutscher Ärzte-Verlag, 5. Aufl. 2004, 473
-
Lion TH, Kovar H: Tumorgenetik, in Gutjahr P: Krebs bei Kindern und Jugendlichen. Deutscher Ärzte-Verlag Köln 5. Aufl. 2004, 10
-
Bielack S, Kempf-Bielack B, Delling G, Exner G, Flege S, Helmke K, Kotz R, Salzer-Kuntschik M, Werner M, Winkelmann W, Zoubek A, Jürgens H, Winkler K: Prognostic factors in high-grade osteosarcoma of the extremities or trunk. J Clin Oncol 2002, 20: 776
-
Bielack S, Flege S, Kempf-Bielack B: Behandlungskonzept des Osteosarkoms. Onkologe 2000, 6: 747 [DOI: 10.1007/s007610070064]
-
Bielack S, Kempf-Bielack B, Schwenzer D, Birkfellner T, Delling G, Ewerbeck V, Exner G, Fuchs N, Göbel U, Graf N, Heise U, Helmke K, von Hochstetter A, Jürgens H, Maas R, Munchow N, Salzer-Kuntschik M, Treuner J, Veltmann U, Werner M, Winkelmann W, Zoubek A, Kotz R: Neoadjuvant therapy for localized osteosarcoma of extremities. Results from the Cooperative osteosarcoma study group COSS of 925 patients. Klin Pädiatr 1999, 211: 260
Другие заболевания из группы Онкологические заболевания:
| Аденома гипофиза |
| Аденома паращитовидных (околощитовидных) желез |
| Аденома щитовидной железы |
| Альдостерома |
| Ангиома глотки |
| Ангиосаркома печени |
| Астроцитома головного мозга |
| Базально-клеточный рак (базалиома) |
| Бовеноидный папулез полового члена |
| Болезнь Боуэна |
| Болезнь Педжета (рак соска молочной железы) |
| Болезнь Ходжкина (лимфогранулематоз, злокачественная гранулема) |
| Внутримозговые опухоли полушарий мозга |
| Волосатый полип глотки |
| Ганглиома (ганглионеврома) |
| Ганглионеврома |
| Гемангиобластома |
| Гепатобластома |
| Герминома |
| Гигантская кондилома Бушке-Левенштейна |
| Глиобластома |
| Глиома головного мозга |
| Глиома зрительного нерва |
| Глиома хиазмы |
| Гломусные опухоли (параганглиомы) |
| Гормонально-неактивные опухоли надпочечников (инциденталомы) |
| Грибовидный микоз |
| Доброкачественные опухоли глотки |
| Доброкачественные опухоли зрительного нерва |
| Доброкачественные опухоли плевры |
| Доброкачественные опухоли полости рта |
| Доброкачественные опухоли языка |
| Злокачественные новообразования переднего средостения |
| Злокачественные новообразования слизистой оболочки полости носа и придаточных пазух |
| Злокачественные опухоли плевры (рак плевры) |
| Карциноидный синдром |
| Кисты средостения |
| Кожный рог полового члена |
| Кортикостерома |
| Костеобразующие злокачественные опухоли |
| Костномозговые злокачественные опухоли |
| Краниофарингиома |
| Лейкоплакия полового члена |
| Лимфома |
| Лимфома Беркитта |
| Лимфома щитовидной железы |
| Лимфосаркома |
| Макроглобулинемия Вальденстрема |
| Медуллобластома головного мозга |
| Мезотелиома брюшины |
| Мезотелиома злокачественная |
| Мезотелиома перикарда |
| Мезотелиома плевры |
| Меланома |
| Меланома конъюнктивы |
| Менингиома |
| Менингиома зрительного нерва |
| Множественная миелома (плазмоцитома, миеломная болезнь) |
| Невринома глотки |
| Невринома слухового нерва |
| Нейробластома |
| Неходжкинская лимфома |
| Облитерирующий ксеротический баланит (склерозирующий лихен) |
| Опухолеподобные поражения |
| Опухоли |
| Опухоли вегетативной нервной системы |
| Опухоли гипофиза |
| Опухоли костей |
| Опухоли лобной доли |
| Опухоли мозжечка |
| Опухоли мозжечка и IV желудочка |
| Опухоли надпочечников |
| Опухоли паращитовидных желез |
| Опухоли плевры |
| Опухоли спинного мозга |
| Опухоли ствола мозга |
| Опухоли центральной нервной системы |
| Опухоли шишковидного тела |
| Остеоидная остеома (остеоид-остеома) |
| Остеома |
| Остеохондрома |
| Остроконечные кондиломы полового члена |
| Папиллома глотки |
| Папиллома полости рта |
| Параганглиома среднего уха |
| Пинеалома |
| Пинеобластома |
| Плоскоклеточный рак кожи |
| Пролактинома |
| Рак анального канала |
| Рак ануса (анальный рак) |
| Рак бронхов |
| Рак вилочковой железы (рак тимуса) |
| Рак влагалища |
| Рак внепеченочных желчных путей |
| Рак вульвы (наружных половых органов) |
| Рак гайморовой пазухи |
| Рак глотки |
| Рак головного мозга |
| Рак гортани |
| Рак губы |
| Рак губы |
| Рак двенадцатиперстной кишки |
| Рак желудка |
| Рак желчного пузыря |
| Рак конъюнктивы |
| Рак лёгкого |
| Рак матки |
| Рак маточной (фаллопиевой) трубы |
| Рак молочной железы (рак груди) |
| Рак мочевого пузыря |
| Рак мошонки |
| Рак паращитовидных (околощитовидных) желез |
| Рак печени |
| Рак пищевода |
| Рак поджелудочной железы |
| Рак полового члена |
| Рак почечной лоханки и мочеточника |
| Рак почки |
| Рак предстательной железы (простаты) |
| Рак придатка яичка |
| Рак прямой кишки (колоректальный рак) |
| Рак среднего уха |
| Рак толстого кишечника |
| Рак тонкого кишечника |
| Рак трахеи |
| Рак уретры (мочеиспускательного канала) |
| Рак шейки матки |
| Рак щитовидной железы |
| Рак эндометрия (рак тела матки) |
| Рак языка |
| Рак яичка |
| Рак яичников |
| Ретикулосаркома |
| Ретинобластома (рак сетчатки) |
| Саркома Юинга |
| Синдром Сезари |
| Соеденительнотканные злокачественные опухоли |
| Соединительнотканные опухоли |
| Сосудстые опухоли |
| Тимома |
| Феохромоцитома |
| Фиброма носоглотки |
| Фиброма полости рта |
| Хемодектома каротидная |
| Хондробластома |
| Хондрома |
| Хондромиксоидная фиброма |
| Хондросаркома |
| Хордома |
| Хориоангиома плаценты |
| Хрящеобразующие злокачественные опухоли |
| Эпендимома головного мозга |
| Эритроплазия Кейра |
| Эстезионейробластома (нейроэпителиома обонятельного нерва) |
Классификация и стадии
Выделяют следующие виды сарком легких:
- Саркома легких низкой степени злокачественности. Она образуется из более зрелых (дифференцированных) клеток. Они не склонны к быстрому делению, как другие виды сарком, поэтому прогрессирование происходит относительно медленно. Сама опухоль преимущественно состоит из стромы, в которой имеются вкрапления злокачественных клеток. Их количество относительно общей массы невелико.
- Саркома со средней степенью злокачественности образуется из клеток низкой степени дифференцировки. В структуре опухоли злокачественные элементы уже имеют преобладающее значение. Помимо этого, имеется хорошее кровоснабжение благодаря разветвленной сосудистой сети. Это способствует раннему метастазированию.
- Саркома легких высокой степени злокачественности образуется из недифференцированных клеток, которые настолько незрелые, что их еще нельзя отнести к какому-либо виду ткани. Они с равной долей вероятности могут стать любой клеткой соединительной ткани. Недифференцированные опухоли легких крайне агрессивны. Они стремительно растут и очень быстро метастазируют, образуя множественные метастатические очаги.
Легкое — это орган, имеющий сложное строение, состоящее из альвеол, бронхиол и бронхов, кровеносных и лимфатических сосудов и других элементов. Все данные структуры имеют клетки соединительной ткани, из которой могут образовываться разные виды высокодифференцированных сарком. Поэтому саркома легкого — это сборное понятие, включающее в себя несколько видов новообразований легких (ангиосаркомы, фибросаркомы и др).
Недифференцированные саркомы разделяют в зависимости от морфологических особенностей клеток:
- Веретеноклеточные.
- Круглоклеточные.
- Полиморфноклеточные.

Лечение
Основным методом лечения лейомиосаркомы является радикальная хирургическая операция. При низкозлокачественных опухолях без метастазов этого бывает достаточно, но при более неблагоприятных прогнозах проводят комбинированное воздействие с помощью облучения и химиотерапии.
Хирургическое лечение
Золотым стандартом лечения лейомиосаркомы является радикальное иссечение опухоли в пределах визуально неизмененных тканей. Раньше это были обширные калечащие операции, которые предполагали ампутации конечностей и внутренних органов. Сегодня с развитием хирургических технологий, предпочтение отдается органосохраняющему лечению. Используются следующие техники вмешательства:
- Широкая резекция. Опухоль иссекается в пределах 5 см незатронутых тканей. Такая техника применяется при лечении кожной лейомиосаркомы и поверхностно расположенных опухолях.
- Широкое иссечение. Опухоль удаляется в пределах тканей одной анатомической зоны с отступом от ее края не менее чем на 4-6 см.
- Футлярно-фасциальное иссечение. Опухоль удаляется в едином мышечно-фасциальном футляре. При этом производят полное удаление вовлеченной мышцы с рассечением места ее прикрепления. Если в процесс вовлекаются нервы и кровеносные сосуды, их также подвергают резекции.
- Ампутации и экзартикуляции — производится полное удаление конечности или ее резекция по линии сустава. Такие вмешательства показаны при высокозлокачественных новообразованиях, которые затронули крупные кровеносные сосуды, мышцы и костные структуры.
После того как лейомиосаркома будет удалена, необходимо ее исследовать на предмет определения наличия злокачественных клеток в краях отсечения. При положительном результате объем вмешательства расширяют или проводят повторные радикальные операции. С целью маркировки полей облучения при проведении последующей лучевой терапии, в ложе удаленной опухоли оставляют специальные клипсы.
Лучевая терапия
Лучевая терапия занимает большое место в лечении лейомиосарком высокой степени злокачественности. Ее проводят в неоадъювантном (дооперационном) и адъювантном (послеоперационном) режимах.
Неоадъювантная ЛТ преследует следующие цели:
- Уменьшение объема опухоли и, как следствие, уменьшение объема хирургической операции.
- Перевод новообразования из неоперабельного в операбельное состояние.
- Снижение риска интраоперационной трансплантации опухоли.
В рамках неоадъювантной ЛТ поле облучения должно захватывать опухоль и рядом расположенные ткани в пределах 3-4 см. Если опухоль сильно большая, зону облучение расширяют до 10 см от ее края. При облучении в области конечностей рекомендуется выстраивать поле облучения таким образом, чтобы оно распространялось не более чем на 2/3 ее окружности. Это снижает риски постлучевых осложнений, например, контрактур, отеков, некрозов.
Однако такой режим лечения имеет и недостатки:
- Задерживается проведение операции из-за потенциальных проблем с ранозаживлением.
- Могут быть проблемы с морфологическим типированием.
- Сложности с определением стадии заболевания и, соответственно, проведение лечения в недостаточном объеме.
В клинической практике чаще используется послеоперационная (адъювантная) лучевая терапия. Она проводится в следующих случаях:
- Лечение высокозлокачественной лейомиосаркомы.
- Повреждение капсулы опухоли в время операции.
- Нерадикальность операции — в краях резекции обнаруживаются злокачественные клетки и нет возможности проведения повторного хирургического вмешательства для достижения радикальности.
Начало адъювантной ЛТ должно быть не позже, чем через 4 недели после операции. Поля облучения должны включать следующие зоны:
- Ложе опухоли.
- Послеоперационный рубец.
- 2 см рядом расположенных тканей.
Суммарная очаговая доза должна составлять 60 Гр, при нерадикальном вмешательстве ее увеличивают до 70 Гр.
Химиотерапия
Химиотерапия назначается в следующих случаях:
- Есть данные о наличии метастазов.
- Нерезектабельные опухоли.
- Отказ пациента от хирургического лечения (в этих случаях показана химиолучевая терапия).
- Лечение высокозлокачественных опухолей.
Химиотерапия может проводиться на дооперационном и в послеоперационном периоде. В первом случае показано проведение 2-3 курсов ХТ с перерывом в 3-4 недели. Послеоперационная химиотерапия, как правило, проводится в объеме 3-4 курсов. В рамках терапии первой линии используются схемы, содержащие доксорубицин. В качестве терапии второй линии применяют комбинацию гемцитабина с доцетакселом.